题目内容
18.生产、生活、科技、环境等都离不开化学.(1)奶制品中含有丰富的钙元素(填“单质”或“元素”),人体每日要摄取足够量的钙,否则会导致D(填字母序号).
A.贫血症 B.坏血病 C.夜盲症D.骨质疏松
(2)用活性炭净水器可净化饮用水是利用活性炭的吸附作用.
(3)石墨能用于制作干电池的电极,是因为石墨具有导电性.
(4)石灰水敞口放置在空气,水面上会出现一层白膜,是因为CO2+Ca(OH)2=CaCO3↓+H2O.
(用化学方程式表示).
(5)小崔同学根据氢氧化钠的性质做硫在氧气中燃烧的实验时,集气瓶内预先加有少量氢氧化钠溶液,其目的是吸收二氧化硫气体;,写出反应的化学方程式SO2+2NaOH=Na2SO3+H2O.
分析 (1)根据奶制品和人体中钙的存在形式判断.
(2)活性炭具有吸附性;
(3)石墨能够导电,可作电极;
(4)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可;
(5)硫在氧气中剧烈燃烧,产生明亮蓝紫色火焰,生成的二氧化硫气体有毒排到空气中会造成污染,利用其可与氢氧化钠反应,在瓶中加入氢氧化钠溶液吸收产生的二氧化硫气体;二氧化硫与氢氧化钠反应生成亚硫酸钠和水.
解答 解:(1)在奶制品中或在人体内,钙是以无机盐的形式存在的,这里的钙是指盐中含有的钙元素;老年人缺钙会患骨质疏松.
(2)用活性炭净水器可净化饮用水是利用活性炭的吸附作用.
(3)石墨能用于制作干电池的电极,是因为石墨具有导电性.
(4)石灰水中的溶质是氢氧化钙,能与空气中的二氧化碳反应生成碳酸钙和水;碳酸钙是一种不溶于水的白色物质,故久盛石灰水的试剂瓶的内壁常附有一层白膜,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.
(5)硫在氧气中剧烈燃烧产生的二氧化硫能与氢氧化钠发生而被氢氧化钠溶液吸收,避免污染;二氧化硫与氢氧化钠反应生成亚硫酸钠和水,反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O
故答案为:(1)元素;D;(2)吸附;(3)导电;(4)CO2+Ca(OH)2=CaCO3↓+H2O.(5)吸收二氧化硫气体;SO2+2NaOH=Na2SO3+H2O
点评 关注生命,呵护健康,是人类不断探求的永恒主题,它既是社会热点,也是重要的中考热点之一.

练习册系列答案
相关题目
14.下列物质的用途不是利用其化学性质的是( )
| A. | 液态氮做制冷剂 | B. | 碘液检验土豆中含有淀粉 | ||
| C. | 氢气做清洁高效的新能源 | D. | 二氧化碳在蔬菜大棚用作气体肥料 |
6.下列不属于缓慢氧化的是( )
| A. | 木材燃烧 | B. | 动植物呼吸 | C. | 酒的酿造 | D. | 白菜腐烂 |
10.人体中缺少某些元素会影响健康,甚至引起疾病.以下疾病可能与缺锌有关的是( )
| A. | 甲状腺肿大 | B. | 骨质疏松 | C. | 贫血 | D. | 侏儒症 |
7.如图为甲、乙两种固体物质在水中的溶解度曲线,下列说法不正确的是( )
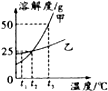

| A. | 甲中混有少量乙时,提纯甲的方法是降温结晶 | |
| B. | 甲、乙物质的溶解度都为25g | |
| C. | t3℃,在150g水中加入80g甲物质,得到溶液的质量为225g | |
| D. | 将t3℃时等质量的甲、乙饱和溶液分别降温到t1℃,则甲溶液的溶质质量分数小于乙 |
8.下列实验操作错误的是( )
| A. | 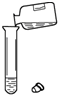 倾倒液体 | B. | 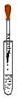 滴加液体 | C. | 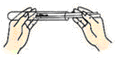 用药勺取用粉末 | D. |  读取液体体积 |