题目内容
7.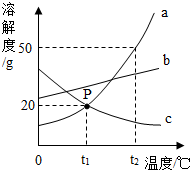 如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )| A. | t2℃时,b物质的溶解度为50g | |
| B. | t1℃时,三种物质饱和溶液的浓度为b>a=c | |
| C. | 接近饱和的c物质,可采用降温的方法使其达到饱和 | |
| D. | t1℃时,a物质饱和溶液溶质质量分数为20% |
分析 根据固体物质的溶解度曲线可以:①查出某物质在某温度下的溶解度,②比较不同的物质在同一温度下的溶解度大小,从而判断在某温度下,不同物质的饱和溶液中溶质的质量分数的大小,溶解度大,则饱和溶液中溶质的质量分数则大,③可知物质的溶解度随温度变化情况,从而判断饱和溶液和不饱和溶液的相互转化方法.
解答 解:A、由溶解度曲线可知,t2℃时,b物质的溶解度小于50g,故错误;
B、t1℃时,三种物质的溶解度大小关系是b>a=c,据饱和时质量分数的计算式$\frac{溶解度}{溶解度+100g}$×100%可知:溶解度大则溶质的质量分数大,所以饱和溶液的浓度大小关系是:b>a=c,正确;
C、由于c的溶解度随温度的升高而减小,所以使接近饱和的c溶液变为饱和,可采取升温的方法,故错误;
D、t1℃时a的溶解度是20g,所以其饱和溶液溶质的质量分数是:$\frac{20g}{120g}$×100%<20%,故错误;
故选:B.
点评 本题难度不是很大,主要考查了固体的溶解度所表示的意义,从而加深学生对固体溶解度的理解,培养学生对知识的灵活应用的能力.

练习册系列答案
相关题目
2.汽车用铅蓄电池中需要质量分数为28%的稀硫酸.若在实验室中用10g质量分数为98%的浓硫酸(密度为1.84g/m3)配制28%的稀硫酸,下列做法或说法正确的是( )
| A. | 将25mL水慢慢倒入盛有54mL浓硫酸的量筒中,并用玻璃棒不断搅拌 | |
| B. | 将10g98%的浓硫酸沿烧杯壁慢慢倒入盛有25mL水的烧杯中,并用玻璃棒不断搅拌 | |
| C. | 将28mL98%的浓硫酸沿烧杯壁慢慢倒入盛有100mL水的烧杯中,并用玻璃棒不断搅拌 | |
| D. | 若其他操作正确,量取25mL水时俯视读数,则所配稀硫酸中溶质的质量分数小于28% |
12.桐桐同学对下列物质燃烧时的现象描述,不正确的是( )
| A. | 铝箔在氧气中燃烧,发出耀眼的光 | |
| B. | 硫在氧气中燃烧,发出明亮的蓝紫色火焰 | |
| C. | 铁丝在氧气中燃烧,火星四射,生成黑色固体物质 | |
| D. | 木炭在氧气中燃烧,发出明亮的白光,并形成白雾 |
19.下列有关实验现象的描述,正确的是( )
| A. | 木炭在氧气中燃烧后生成黑色固体 | |
| B. | 红磷在氧气中燃烧后生成白色五氧化二磷气体 | |
| C. | 细铁丝在空气中燃烧,火星四射,生成一种黑色固体物质 | |
| D. | 硫磺在空气中燃烧,生成一种具有刺激性气味的气体 |
16.对于Fe、Fe2+、Fe3+三种微粒的判断,不正确的是( )
| A. | 核电荷数相等 | B. | 质量几乎相等 | ||
| C. | 属同一种元素 | D. | 属于铁的三种同位素 |
 普通黄铜仅由铜和锌组成,现有一块黄铜样品的质量为50克,某学习小组利用一种未知溶质质量分数的稀盐酸来测定锌铜合金中铜的质量分数.实验中样品与酸充分反应,样品的质量变化情况如图所示.
普通黄铜仅由铜和锌组成,现有一块黄铜样品的质量为50克,某学习小组利用一种未知溶质质量分数的稀盐酸来测定锌铜合金中铜的质量分数.实验中样品与酸充分反应,样品的质量变化情况如图所示.