题目内容
在宏观、微观、符号之间建立联系,是化学学科特有的思维方式.
(1)在C60、金刚石、氢氧化钠三种物质中,由分子构成的物质是 .
(2)据报道,某药企生产的胶囊中“铬”超标,长期服用会引起“铬中毒”.
铬元素的相关信息如图1所示.请回答:
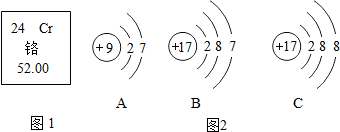
铬元素的相对原子质量为 ;铬原子核外电子数为 .铬原子失去3个电子所形成的离子符号为 ;铬元素属 (填“金属”或“非金属”)元素.
(3)如图2为A、B、C三种粒子的结构示意图,其中属同种元素的粒子是 (填字母),A和B两种
粒子的 相同,所以它们具有相似的化学性质.A元素位于周期表的第 周期.
(4)如图分别表示不同的化学反应.
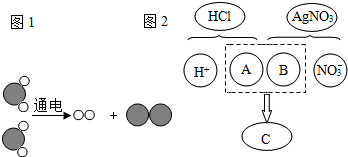
①图1是电解水微观模型图,根据质量守恒定律可知该模型图中缺少了 (填字母序号)

②图2描述了稀盐酸与硝酸银溶液反应的微观实质,C处应填入的符号为 .
(1)在C60、金刚石、氢氧化钠三种物质中,由分子构成的物质是
(2)据报道,某药企生产的胶囊中“铬”超标,长期服用会引起“铬中毒”.
铬元素的相关信息如图1所示.请回答:

铬元素的相对原子质量为
(3)如图2为A、B、C三种粒子的结构示意图,其中属同种元素的粒子是
粒子的
(4)如图分别表示不同的化学反应.

①图1是电解水微观模型图,根据质量守恒定律可知该模型图中缺少了

②图2描述了稀盐酸与硝酸银溶液反应的微观实质,C处应填入的符号为
考点:分子、原子、离子、元素与物质之间的关系,中和反应及其应用,微粒观点及模型图的应用,原子结构示意图与离子结构示意图,元素周期表的特点及其应用
专题:化学反应模拟图型,物质的微观构成与物质的宏观组成,化学用语和质量守恒定律
分析:(1)根据构成物质的三种基本粒子来分析;
(2)根据元素周期表能够提供的信息来分析解答;
(3)根据元素的含义可知具有相同质子数的原子为同一类元素以及元素的化学性质取决于最外层电子数进行解答;
(4)根据化学变化的实质来分析解答.
(2)根据元素周期表能够提供的信息来分析解答;
(3)根据元素的含义可知具有相同质子数的原子为同一类元素以及元素的化学性质取决于最外层电子数进行解答;
(4)根据化学变化的实质来分析解答.
解答:解:(1)C60是由C60分子构成的,金刚石是由碳原子构成的,氢氧化钠是由钠离子和氢氧根离子构成的;
(2)在元素周期表这一小格中,正下方的数字表示铬元素的相对原子质量为52.00,左上角的数字是其原子序数,等于其质子数,也等于其核外电子数,故铬原子核外电子数为24;铬原子失去3个电子,带3个单位的正电荷,故离子符号为:Cr3+;由“铬”元素名称可知属于金属元素.
(3)核电荷数或质子数决定元素种类,最外层电子数决定元素的化学性质,原子核外有几个电子层,在元素周期表中就位于第几周期;
(4)①根据质量守恒定律分析可知,电解水时,每两个水分子会产生两个氢分子和一个氧分子,故缺少一个氢分子,选B;
②稀盐酸与硝酸银溶液反应属于复分解反应,根据反应实质可知,盐酸中的氯离子与硝酸银中的银离子结合成氯化银白色沉淀.
故答案为:(1)C60;
(2)52.00;24; Cr3+;金属;
(3)BC;最外层电子数; 二;
(4)①B;②AgCl.
(2)在元素周期表这一小格中,正下方的数字表示铬元素的相对原子质量为52.00,左上角的数字是其原子序数,等于其质子数,也等于其核外电子数,故铬原子核外电子数为24;铬原子失去3个电子,带3个单位的正电荷,故离子符号为:Cr3+;由“铬”元素名称可知属于金属元素.
(3)核电荷数或质子数决定元素种类,最外层电子数决定元素的化学性质,原子核外有几个电子层,在元素周期表中就位于第几周期;
(4)①根据质量守恒定律分析可知,电解水时,每两个水分子会产生两个氢分子和一个氧分子,故缺少一个氢分子,选B;
②稀盐酸与硝酸银溶液反应属于复分解反应,根据反应实质可知,盐酸中的氯离子与硝酸银中的银离子结合成氯化银白色沉淀.
故答案为:(1)C60;
(2)52.00;24; Cr3+;金属;
(3)BC;最外层电子数; 二;
(4)①B;②AgCl.
点评:本题考查了对物质的结构、元素周期表中的一个小格所提供的信息的了解情况,微观反应过程及原子结构示意图所表示出的信息和意义.

练习册系列答案
相关题目
物质的俗名、化学式及所属类别都正确的是( )
| A、大理石 CaCO3 酸 |
| B、纯碱 Na2CO3 碱 |
| C、熟石灰 Ca(OH)2 碱 |
| D、烧碱 NaOH 盐 |


 安徽江淮汽车第四代纯电动汽车今年将有500辆出租车投放使用.如图为江汽纯电动汽车实物图,请据图回答下列问题.
安徽江淮汽车第四代纯电动汽车今年将有500辆出租车投放使用.如图为江汽纯电动汽车实物图,请据图回答下列问题.