题目内容
17.氧化钙和碳酸钙的固体混合物质量为100g,将其高温煅烧至碳酸钙完全分解,称得剩余固体的质量为70g.则原固体混合物中钙元素的质量分数为( )| A. | 20% | B. | 40% | C. | 50% | D. | 70% |
分析 根据碳酸钙完全分解,则剩余固体为氧化钙,利用钙元素的质量守恒可知混合物中钙元素的质量,再计算原固体混合物中钙元素的质量分数.
解答 解:解:因反应后得到的固体物质是纯净的CaO,
由高温煅烧过程中钙元素的质量不发生变化,
则CaO中钙元素的质量就是原混合物中钙元素的质量,
CaO中钙元素的质量为70×$\frac{40}{40+16}$×100%=50g,
则原固体混合物中钙元素的质量分数是$\frac{50g}{100g}$×100%=50%,
故选C.
点评 本题考查元素的质量分数计算,学生利用碳酸钙完全分解后固体为氧化钙,再利用钙元素的质量守恒来推断混合物中钙元素的质量是解答的关键.

练习册系列答案
相关题目
17.下列实验操作中,正确的是( )
| A. |  | B. |  | C. |  | D. |  |
18.某化学兴趣小组的同学在实验室发现以前用的一瓶氢氧化钠溶液忘记了盖瓶塞,他们取这种氢氧化钠溶液少量于试管中,再逐滴加入稀盐酸,观察到有气泡产生.小组中有同学断定,这瓶氢氧化钠溶液已经变质.辅导老师肯定了该同学的看法,又有同学提出:所用氢氧化钠溶液是否完全变质?兴趣小组的同学在辅导老师的鼓励下又进行了如下的实验探究:
【提出问题】氢氧化钠溶液是否完全变质?
【进行猜想】(1)该氢氧化钠溶液部分变质;(2)该氢氧化钠溶液全部变质.
【查阅资料】氯化钡溶液呈中性.
【设计并进行实验】
【结论】该小组同学所用的氢氧化钠溶液是部分(填“部分”或者“全部”)变质.
【反思】氢氧化钠溶液露置于空气中容易变质,反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O.
【提出问题】氢氧化钠溶液是否完全变质?
【进行猜想】(1)该氢氧化钠溶液部分变质;(2)该氢氧化钠溶液全部变质.
【查阅资料】氯化钡溶液呈中性.
【设计并进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量该瓶氢氧化钠溶液于水管中,向溶液中滴加过量的BaCl2溶液,并不断振荡 | 有 白色沉淀产生 | 说明原溶液中一定有碳酸钠 |
| (2)取步骤(1)试管中的少量上层清液,向其中滴加酚酞试液 | 发现溶液变红色 | 说明原溶液中一定有 氢氧化钠. |
【反思】氢氧化钠溶液露置于空气中容易变质,反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O.
2.研究小组对氯水(氯气的水溶液)为进行探究.
(1)测定氯水的酸性:取少量,向其中滴加(选填指示字母)b,一开始应观察到滴加的指示剂在氯水中红色.
a.无色酚酞试液 b.紫色石蕊试液
(2)氯水具有漂白性,请你参与“氯水使品红试纸褪色”的研究.
【提出问题】氯水中的什么成分使品红试纸褪色?
【猜想】
猜想1:氯水中的水使品红试纸褪色.
猜想2:氯水中的Cl2使品红试纸褪色.
猜想3:氯水中的HCl使品红试纸褪色.
猜想4:氯水中的HClO(填化学式)使品红试纸褪色.
【实验探究】
【结论】通过探究,找到了氯水中使水使品红试纸褪色的原因.
【思考】实验(1)向氯水中滴加几滴所选指示剂后,最终观察到的现象是先变红色后褪色.
(1)测定氯水的酸性:取少量,向其中滴加(选填指示字母)b,一开始应观察到滴加的指示剂在氯水中红色.
a.无色酚酞试液 b.紫色石蕊试液
(2)氯水具有漂白性,请你参与“氯水使品红试纸褪色”的研究.
【提出问题】氯水中的什么成分使品红试纸褪色?
【猜想】
猜想1:氯水中的水使品红试纸褪色.
猜想2:氯水中的Cl2使品红试纸褪色.
猜想3:氯水中的HCl使品红试纸褪色.
猜想4:氯水中的HClO(填化学式)使品红试纸褪色.
【实验探究】
| 实验操作 | 实验现象 | 结论 |
| ①用水润湿品红试纸,观察 | 试纸不褪色 | 猜想1不成立 |
| ②把品红试纸放入干燥的氯气中,观察 | 试纸不褪色 | 猜想2不成立 |
| ①把品红试纸放入盐酸中,观察 | 试纸不褪色 | 猜想3不成立 |
【思考】实验(1)向氯水中滴加几滴所选指示剂后,最终观察到的现象是先变红色后褪色.
9.下列实验中,根据现象得出的结论,正确的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | CO2通入紫色石蕊试液 | 石蕊试液变红 | CO2具有酸的性质 |
| B | 黄豆和芝麻混合后振荡 | 总体积变小 | 分子之间有空隙 |
| C | 稀H2SO4溶液中滴入NaOH溶液 | 无明显现象 | H2SO4和NaOH没有发生化学变化 |
| D | 冷却CuSO4热饱和溶液 | 有晶体析出 | CuSO4的溶解度随温度降低而减小 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
6.氢气和一氧化碳、木炭一样具有还原性,能使氧化铜还原成铜,反应的化学方程式为:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.该反应属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
7.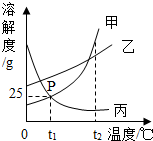 如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是( )
如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是( )
 如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是( )
如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是( )| A. | t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1:4 | |
| B. | P点表示甲、丙两种物质的饱和溶液质量相等 | |
| C. | t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液 | |
| D. | 将三种物质的溶液从t2℃降至t1℃,析出晶体最多的是甲物质 |