题目内容
3.下列说法不正确的是( )| A. | 镁铝合金mg和足量的盐酸反应生成H20.1g,则m可能是0.8 | |
| B. | 常温下,将5.6g生石灰放入94.4g水中,所得溶液中溶质质量分数小于1% | |
| C. | 将镁粉和铝粉的混合物7.2g与足量的氧气充分反应,得到的氧化物质量可能为13.6g | |
| D. | 将铁合金置于氧气中燃烧得到0.44g二氧化碳和29g四氧化三铁,则铁合金是钢 |
分析 A、根据镁和盐酸、铝和盐酸反应的化学方程式,采用极值法进行计算;
B、生石灰与水发生化学反应生成了氢氧化钙,然后根据氢氧化钙的微溶性来分析;
C、根据这两种金属与氧气反应,如果全用铝,则得到的氧化物质量13.6g,如果全为镁,得到的氧化物质量12g,所以混合金属得到的氧化物质量取值范围为12g~13.6g;
D、根据生成二氧化碳、四氧化三铁的质量求出碳元素的质量和铁元素质量,然后求出碳元素的质量分数,确定该铁合金的类别.
解答 解:A、设生成0.1g氢气需要镁的质量为x,需要铝的质量为y
Mg+2HCl=MgCl2+H2↑
24 2
x 0.1g
$\frac{24}{x}=\frac{2}{0.1g}$
x=1.2g
2Al+6HCl=2AlCl3+3H2↑
54 6
y 0.1g
$\frac{54}{y}=\frac{6}{0.1g}$
y=0.9g
所以镁铝合金mg和足量的盐酸反应生成H20.1g,则m在0.9~1.2之间,不可能是0.8,故A不正确;
B、生石灰溶解于水会和水反应:CaO+H2O=Ca(OH)2,Ca(OH)2的溶解度曲线: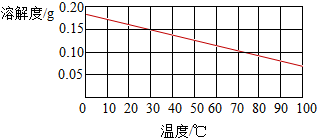
由于Ca(OH)2的溶解度很小,不会超过0.2g,所以质量分数不会大于1%,所以溶液质量分数很小;故B正确;
C、设,7.2g镁与足量氧气反应产生氧化镁的质量为x,7.2g铝与足量氧气反应产生氧化铝的质量为y;
2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO,4Al+3O2$\frac{\underline{\;点燃\;}}{\;}$2Al2O3
48 80 108 204
7.2g x 7.2g y
$\frac{48}{7.2g}=\frac{80}{x}$,$\frac{108}{7.2g}=\frac{204}{y}$
x=12g,y=13.6g
由此可见,若全部为铝,则得到的氧化物质量13.6g,如果全为镁,得到的氧化物质量12g,由于是混合物,因此混合物得到的氧化物质量应介于12g与13.6g之间,故C不正确;
D、根据质量守恒定律,化学反应前后元素的质量不变,故碳元素的质量为:0.44g×$\frac{12}{44}$×100%=0.12g,铁元素的质量为:29g×$\frac{168}{232}$×100%=21g,故合金中碳元素的质量分数为:$\frac{0.12g}{21g+0.12g}$×100%=0.57%,钢中的含碳量为:0.03%~2%,故属于钢,故D正确.
故选:AC.
点评 本题主要考查了化学方程式的计算和化学式的计算,难度较大,注意解题的规范性和准确性.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案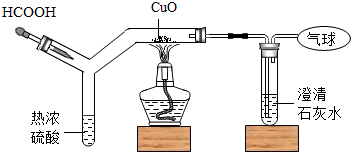 如图为CO还原CuO“微型”实验装置(夹持仪器等略),已知:HCOOH$\frac{\underline{\;热浓硫酸\;}}{\;}$H2O+CO↑,下列说法错误的是( )
如图为CO还原CuO“微型”实验装置(夹持仪器等略),已知:HCOOH$\frac{\underline{\;热浓硫酸\;}}{\;}$H2O+CO↑,下列说法错误的是( )| A. | 实验中所需CO可现制现用 | |
| B. | 此装置可节约用品,污染小,现象明显 | |
| C. | 此装置内空间较小,空气易排空,实验危险系数小 | |
| D. | 该实验中所涉及反应的基本类型有分解反应和置换反应 |
(1)某地区学生营养午餐摄入标准值(每人每天)如表所示.
| 能量 | 3890kJ |
| 蛋白质 | 48g |
| 脂肪 | 30g |
| 钙 | 480mg |
| 锌 | 6mg |
| 铁 | 4mg |
| 维生素 | 24mg |
②人体不可缺少的营养物质有蛋白质、糖类、脂肪、维生素、水和矿物质;
(2)材料对我们生活的影响越来越大,下列属于合成材料的是bd.(填序号)
a.镁铝合金 b.聚乙烯 c.钢筋混凝土 d.有机玻璃.
| A. | 1个铁离子-Fe2+ | |
| B. | 氧化镁-MgO2 | |
| C. | 2个氮原子-N2 | |
| D. | 氯酸钾中氯元素的化合价为$\stackrel{+5}{KCl{O}_{3}}$ |
| A. | 液氮可用作制冷剂 | B. | 氦气可用于制造低温环境 | ||
| C. | 氧气可用作火箭发射的燃料 | D. | 二氧化碳是一种温室气体 |

依据实验过程和出现的现象请你回答下列问题:
(1)气体F的化学式是NH3.
(2)写出步骤①中生成气体B的化学方程式BaCO3+2HCl=BaCl2+H2O+CO2↑.
(3)在溶液C和溶液G中,一定都存在的阴离子是Cl一(写离子符号).
(4)固体混合物A中,肯定不存在的物质有2种,若要进一步推理A的组成,可用溶液D再做实验确定可能含有的物质:
| 实验操作 | 实验现象 | 实验结论 |
| 取溶液D少许,滴加 Na2SO4溶液,震荡 | 有白色沉淀生成 | |
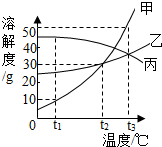 如图是甲、乙、丙三种固体物质在水中的溶解度曲线.下列说法不正确的是( )
如图是甲、乙、丙三种固体物质在水中的溶解度曲线.下列说法不正确的是( )| A. | t1℃时,甲、乙、丙溶解度大小顺序是丙>乙>甲 | |
| B. | t3℃时,将甲、乙饱和溶液降温至t2℃,所得溶液中溶质的质量分数相等 | |
| C. | t1℃时,将甲、丙饱和溶液恒温蒸发10g水后,前者析出晶体而后者无晶体析出 | |
| D. | t3℃时,8g甲中加20g水,充分溶解后再降温到t2℃,所得溶液为饱和溶液 |
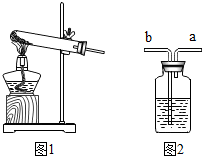 早期的课本里做硫与铁反应的实验方法是:将硫粉与铁粉混合后平铺在石棉网上,再用一根加热过的玻璃棒插入混合物,开始反应后立即拔出玻璃棒,结果可看到反应继续进行,直到反应完全.现在课本里反应改成了将混合物装进试管里,然后用酒精灯加热使其发生反应,如图1.请回答下列问题:
早期的课本里做硫与铁反应的实验方法是:将硫粉与铁粉混合后平铺在石棉网上,再用一根加热过的玻璃棒插入混合物,开始反应后立即拔出玻璃棒,结果可看到反应继续进行,直到反应完全.现在课本里反应改成了将混合物装进试管里,然后用酒精灯加热使其发生反应,如图1.请回答下列问题: