题目内容
1molH2O通电后完全分解得到多少mol的氧气?要使这些氧气完全用于甲烷的燃烧,需要甲烷多少克?请通过计算回答.
【答案】分析:依据物质的量与质量间的转化关系结合方程式的有关计算解答即可;
解答:解:设1molH2O通电后完全分解得到氧气的物质的量是x
2H2O 2H2↑+O2↑
2H2↑+O2↑
2 1
1mol x
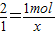
x=0.5mol
这些氧气的质量为0.5mol×32g/mol=16g
设要使这些氧气完全用于甲烷的燃烧,需要甲烷的质量是y
CH4+2O2 CO2+2H2O
CO2+2H2O
16 64
y 16g
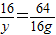
y=4g
答:1molH2O通电后完全分解得到0.5mol的氧气,要使这些氧气完全用于甲烷的燃烧,需要甲烷4克;
点评:本题主要考查化学方程式的书写和有关化学方程式的计算,难度较小.解题时要注意物质的量与质量间的关系转化.
解答:解:设1molH2O通电后完全分解得到氧气的物质的量是x
2H2O
 2H2↑+O2↑
2H2↑+O2↑2 1
1mol x
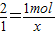
x=0.5mol
这些氧气的质量为0.5mol×32g/mol=16g
设要使这些氧气完全用于甲烷的燃烧,需要甲烷的质量是y
CH4+2O2
 CO2+2H2O
CO2+2H2O16 64
y 16g
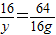
y=4g
答:1molH2O通电后完全分解得到0.5mol的氧气,要使这些氧气完全用于甲烷的燃烧,需要甲烷4克;
点评:本题主要考查化学方程式的书写和有关化学方程式的计算,难度较小.解题时要注意物质的量与质量间的关系转化.

练习册系列答案
相关题目