题目内容
10.表是某地市场销售的“加碘食盐”包装袋上的部分文字说明.| 配料 | 氯化钠、碘酸钾 |
| 含碘量 | (20mg~40mg)/kg |
| 贮藏指南 | 避热、避光、密封 |
| 食用方法 | 勿长时间炖炒 |
(2)由贮藏指南可推测碘酸钾的化学性质有A.
A.受热时易反应 B.见光时比较稳定 C.化学性质比较活泼.
分析 (1)根据碘酸钾的化学性质来分析;
(2)烹调时待食品熟后再加入碘盐,说明碘盐的热稳定性差,受热容易分解.
解答 解:(1)碘盐不能长时间炖炒,这说明碘酸钾受热易分解,所以炖鸡汤时,要等到出锅时添加碘盐;故填:鸡汤出锅时;
(2)由食用方法说明可知,碘酸钾在受热时易分解.故填:A.
点评 本题主要考查盐的概念,解答时要分析各种物质的组成,然后再根据盐概念的含义进行分析、判断,从而得出正确的结论.同时要善于从说明中总结物质的性质.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
20.下列说法正确的是( )
| A. | 物理变化中不一定发生化学变化 | |
| B. | 蓄电池充电时,电能转变成化学能 | |
| C. | 有颜色改变的变化的可能是物理变化 | |
| D. | 有颜色改变的变化一定是化学变化 |
5.下列有关质量守恒定律的理解,正确的是( )
| A. | 5g铁和5g铜混合,物质的总质量为10g,遵守质量守恒定律 | |
| B. | 化学反应前后分子的总数一定不会发生改变 | |
| C. | 5g硫和5g氧气完全反应,生成物质量为10g,遵守质量守恒定律 | |
| D. | 镁条燃烧后质量增加,未遵守质量守恒定律 |
15. 向100g质量分数分别为3.65%盐酸和12%MgSO4的混合溶液中,滴加质量分数为3.42%的Ba(OH)2溶液至过量.(为便于计算设Ba(OH)2溶液的密度为1g/cm3)
向100g质量分数分别为3.65%盐酸和12%MgSO4的混合溶液中,滴加质量分数为3.42%的Ba(OH)2溶液至过量.(为便于计算设Ba(OH)2溶液的密度为1g/cm3)
(1)将产生不同沉淀阶段的沉淀的化学式与加入Ba(OH)2溶液体积(V)的关系填入下表:
(2)请在如图坐标系中完成沉淀的质量和Ba(OH)2溶液体积(V)间的关系图线.
 向100g质量分数分别为3.65%盐酸和12%MgSO4的混合溶液中,滴加质量分数为3.42%的Ba(OH)2溶液至过量.(为便于计算设Ba(OH)2溶液的密度为1g/cm3)
向100g质量分数分别为3.65%盐酸和12%MgSO4的混合溶液中,滴加质量分数为3.42%的Ba(OH)2溶液至过量.(为便于计算设Ba(OH)2溶液的密度为1g/cm3)(1)将产生不同沉淀阶段的沉淀的化学式与加入Ba(OH)2溶液体积(V)的关系填入下表:
| Ba(OH)2溶液体积(V)/mL | ||||
| 沉淀的化学式 |
2.下列方法不能将二氧化碳气体和一氧化碳气体区分开的是( )
| A. | 分别插入燃着的木条;观察现象 | |
| B. | 分别通入碳酸钠溶液中;观察现象 | |
| C. | 分别通入紫色石蕊试液中;观察现象 | |
| D. | 分别通过灼热的氧化铜;观察现象 |
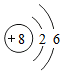 ;根据氧原子结构示意图可知,氧原子在化学反应中易得到(选填“得到”“失去”)电子达到稳定结构.
;根据氧原子结构示意图可知,氧原子在化学反应中易得到(选填“得到”“失去”)电子达到稳定结构.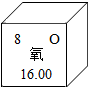 所示,从图中能直接获得的信息是AD.
所示,从图中能直接获得的信息是AD.