题目内容
17.某酸(甲)和某碱(乙)的相对分子质量分别为M1和M2,甲,乙两溶液溶质质量分数相等,当m g甲和n g乙混合后,溶液的pH<7,当m g甲和2n g乙混合后,溶液的pH=7,下列各组物质满足上述情况的是( )| A. | HCl和NaOH | B. | H2SO4和NaOH | C. | H2SO4和Ba(OH)2 | D. | HCl和Ca(OH)2 |
分析 由题意知甲,乙两溶液溶质质量分数相等,当甲、乙两溶液的质量比为m:n时,充分反应后溶液的pH<7,结合化学方程式的意义可以知道,说明此时酸性物质是过量的,而当甲乙两物质按m:2n时的质量比恰好完全中和,结合上述分析可以知道所需碱性物质的分子个数是酸性物质的分子个数的二倍,据此可以知道:只要分别写出下列反应的化学方程式即可得出答案.
解答 解:A、NaOH和HCl反应的化学方程式为:NaOH+HCl═NaCl+H2O,恰好完全反应时NaOH的分子个数是HCl的个数比为1:1,不符合要求,故错误.
B、NaOH和H2SO4反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O,恰好完全反应时NaOH的分子个数是H2SO4的分子个数的二倍,不符合要求,故正确.
C、氢氧化钡和硫酸的反应的化学方程式为:Ba(OH)2+H2SO4═BaSO4↓+2H2O,恰好完全反应时氢氧化钡和硫酸的个数比为1:1,不符合要求,故错误;
D、氢氧化钡和盐酸反应的化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O,恰好完全反应时酸的分子个数是碱的二倍,符合刚才的分析,故错误.
故选B
点评 本题考查了酸和碱之间反应的质量关系,完成此题,可以依据反应的化学方程式和质量守恒定律进行解答

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
8.以下推理合理的是( )
| A. | 含碳元素的物质充分燃烧会有CO2生成,则燃烧能生成CO2的物质一定含碳元素 | |
| B. | 化合物是由不同种元素组成的物质,则由不同种元素组成的物质一定是化合物 | |
| C. | 酸是含有氢元素的化合物,则含有氢元素的化合物一定是酸 | |
| D. | 碳酸盐与稀盐酸反应放出气体,则与稀盐酸反应放出气体的物质一定是碳酸盐 |
5.下列有关能源的叙述正确的是( )
| A. | 石油是一种可再生资源 | |
| B. | 大量使用化石能源会造成大气污染,因此应该停止化石能源的开采和利用 | |
| C. | 人类需要的能量都是由化学反应产生的 | |
| D. | 目前没有大量使用氢能源,是由于氢气的制取成本高,贮存困难 |
2.下列实验操作正确的是( )
| A. | 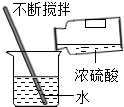 稀释浓硫酸 | B. | 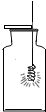 铁丝在氧气中燃烧 | ||
| C. | 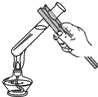 给试管内液体加热 | D. | 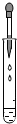 滴加液体 |
16.下列叙述正确的是( )
| A. | 氮气的化学性质不活泼,常用作保护气 | |
| B. | 酸雨的pH小于7,pH小于7的雨水一定是酸雨 | |
| C. | 催化剂能加快化学反应速率 | |
| D. | 溶液中有晶体析出,其溶质质量减小,所以溶质的质量分数一定减小 |
17.茶叶中含有的茶氨酸(C7H14O3N2)可以降低血压、提高记忆力、保护神经细胞等.下列有关茶氨酸的说法中,正确的是( )
| A. | 一个茶氨酸分子中含有一个氮分子 | |
| B. | 茶氨酸属于有机高分子化合物 | |
| C. | 茶氨酸中碳元素与氢元素的质量比为6:1 | |
| D. | 茶氨酸中氢元素的质最分数最大 |