题目内容
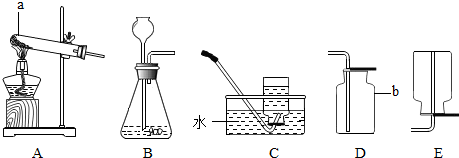
5. 2010年5 月12 日,在苍茫海水中沉没了 800 多年的“南海一号”重见天日,其中的宋代铜钱已经锈迹斑斑.已知:铜绿的主要成分是碱式碳酸铜[Cu 2( OH )2CO3],它受热分解的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$ 2CuO+H2O+CO2↑.某同学设计了如下实验,用来测定碱式碳酸铜受热分解后产生的水和二氧化碳的质量比.实验用到的主要装置如下:
2010年5 月12 日,在苍茫海水中沉没了 800 多年的“南海一号”重见天日,其中的宋代铜钱已经锈迹斑斑.已知:铜绿的主要成分是碱式碳酸铜[Cu 2( OH )2CO3],它受热分解的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$ 2CuO+H2O+CO2↑.某同学设计了如下实验,用来测定碱式碳酸铜受热分解后产生的水和二氧化碳的质量比.实验用到的主要装置如下:(1)装置连接顺序为:②①③.(填写编号)
(2)操作步骤及数据处理:
第一步检查气密性;
第二步装入药品,称取装置 ①和 ③的质量;
第三步连接并固定装置,然后加热固体;
第四步实验后再次称取装置 ①和 ③的质量,记录数据如下:
| 装置 质量 时间 | 装置① | 装置③ |
| 实验前 | 220.0克 | 195.0克 |
| 实验后 | 222.1克 | 199.4克 |
(3)结果分析:从下列选项中选出产生该实验结果可能的原因有哪些?AC
A.二氧化碳没有被完全吸收 B.水没有被完全吸收
C.碱式碳酸铜药品中含有水分 D.碱式碳酸铜没有完全分解.
分析 浓硫酸能够吸收水蒸气,氢氧化钠溶液能够吸收二氧化碳;
根据提供的数据可以进行相关方面的判断.
解答 解:(1)装置连接顺序为②①③.
故填:②①③.
(2)根据以上数据可得产生的水的质量为:222.1g-220.0g=2.1g,产生二氧化碳的质量为:199.4g-195.0g=4.4g,产生的水和二氧化碳的质量之比为:2.1g:4.4g=21:44.
故填:21:44.
(3)A.二氧化碳没有被完全吸收时,会导致测定结果偏大;
B.水没有被完全吸收时,会导致测定结果偏小;
C.碱式碳酸铜药品中含有水分,会导致测定结果偏大;
D.碱式碳酸铜是否完全分解不影响测定结果.
故填:AC.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
16.某化学兴趣小组的同学们对部分日常生活用品的酸碱度进行了测定,他们对每种待测液都做了三次测定,然后取平均值,这样做的目的是提高测定pH的准确性(或减小实验误差).
分析测定结果发现各类洗发液酸碱性差别较大,pH约在7~9之间,护发素的pH均略小于7.同学们联想到洗发、护发的程序,决定探究溶液的酸碱度对头发的影响.
【提出问题】溶液的酸碱度对头发有什么影响?
【设计问题】(1)收集某人的5束头发,分别放入不同pH溶液的烧杯中,静置约30min.
(2)将各束头发取出,用纸巾吸干液体后观察并实验,结果如下表:
【实验结论】碱性溶液对头发影响大,酸性溶液对头发没有明显影响(或溶液碱性越强对头发的影响越大.).
【分析交流】洗发时使用洗发液和护发素的顺序是先用洗发液后用护发素.原因是护发素与洗发液发生中和反应,使头发处于中性或弱酸性的环境中,有利于头发的健康.
【知识拓展】若取用其他人的头发重复上述实验,是(填“是”、“否”)也得出上述实验结论?说明原因:因为头发的主要成分相同.
分析测定结果发现各类洗发液酸碱性差别较大,pH约在7~9之间,护发素的pH均略小于7.同学们联想到洗发、护发的程序,决定探究溶液的酸碱度对头发的影响.
【提出问题】溶液的酸碱度对头发有什么影响?
【设计问题】(1)收集某人的5束头发,分别放入不同pH溶液的烧杯中,静置约30min.
(2)将各束头发取出,用纸巾吸干液体后观察并实验,结果如下表:
| 在不同pH溶液中浸泡后 | |||||
| pH=1 | pH=4 | pH=7 | pH=10 | pH=13 | |
| 头发光泽 | 无明显变化 | 无明显变化 | 无明显变化 | 黄 | 黄、无光泽 |
| 头发拉断难易程度 | 不易断 | 不易断 | 不易断 | 易断 | 极脆 |
【分析交流】洗发时使用洗发液和护发素的顺序是先用洗发液后用护发素.原因是护发素与洗发液发生中和反应,使头发处于中性或弱酸性的环境中,有利于头发的健康.
【知识拓展】若取用其他人的头发重复上述实验,是(填“是”、“否”)也得出上述实验结论?说明原因:因为头发的主要成分相同.
17.小李和小刚正在做实验:在室温下,他们向200g硝酸钾溶液中加入5g硝酸钾固体,充分搅拌,发现尚有约2g固体未溶解.再加入20mL水后,固体全部溶解.下面是两个同学实验后得到的一些结论,其中不正确的是( )
| A. | 原200 g溶液一定是不饱和溶液 | |
| B. | 加入固体搅拌后得到的一定是饱和溶液 | |
| C. | 固体不能全部溶解或有固体析出的溶液一定是饱和溶液 | |
| D. | 加水后得到的一定是不饱和溶液 |
14.下列反应中,属于复分解反应的是( )
| A. | Mg+2HCl═MgCl2+H2↑ | B. | NaCl+AgNO3═AgCl↓+NaNO3 | ||
| C. | H2CO3═H2O+CO2↑ | D. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$ 2H2O |
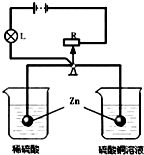 如图所示,R是滑动变阻器,它的金属滑片垂直固定在等臂金属杠 杆的中央且可以随杠杆左右移动.(移动方向与杠杆运动方向一致)杠杆两端分别悬挂等质量、等体积的金属锌球,此时杠杆平衡.再将锌球同时分别浸没到密度相同的稀硫酸和硫酸铜溶液中.反应一段时间后会观察到:
如图所示,R是滑动变阻器,它的金属滑片垂直固定在等臂金属杠 杆的中央且可以随杠杆左右移动.(移动方向与杠杆运动方向一致)杠杆两端分别悬挂等质量、等体积的金属锌球,此时杠杆平衡.再将锌球同时分别浸没到密度相同的稀硫酸和硫酸铜溶液中.反应一段时间后会观察到: