题目内容
1.科学探究是学习化学的一个重要途径,实验是科学探究的重要手段.下列化学实验操作错误的是( )| A. |  | B. |  | C. |  | D. |  |
分析 A、根据蒸发操作的注意事项进行分析判断即可.
B、根据使用胶头滴管滴加少量液体的方法进行分析判断.
C、根据检查装置气密性的方法进行分析判断.
D、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断.
解答 解:A、蒸发时,应用玻璃棒不断搅拌,以防液体受热不均匀,造成液体飞溅,图中所示操作正确.
B、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作正确.
C、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确.
D、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作错误.
故选:D.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
11.根据反应3NO2+H2O→2HNO3+X,推断X的化学式为( )
| A. | N2 | B. | NO | C. | NH3 | D. | N2O5 |
12.用分子的相关知识解释生活中的现象,下列说法正确的是( )
| A. | 冰融化成水,说明分子种类发生改变 | |
| B. | 分离液态空气制氧气说明分子可以再分 | |
| C. | “酒香不怕巷子深”说明分子在不断运动 | |
| D. | 压瘪的乒乓球放入热水中重新鼓起是因为分子体积增大 |
9.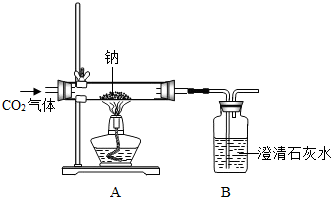 某化学课外兴趣小组为探究Na与CO2的反应进行了如下实验(实验部分装置如图所示):向盛有Na的装置A中通入纯净、干燥的CO2,当观察到装置B中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,Na剧烈燃烧,产生白烟,燃烧结束后装置A中有黑色固体和白色固体生成.
某化学课外兴趣小组为探究Na与CO2的反应进行了如下实验(实验部分装置如图所示):向盛有Na的装置A中通入纯净、干燥的CO2,当观察到装置B中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,Na剧烈燃烧,产生白烟,燃烧结束后装置A中有黑色固体和白色固体生成.
【资料卡】
(1)K、Ca、Na等活泼金属的氧化物均可与水反应生成对应的碱;
(2)钠为银白色金属,过氧化钠为淡黄色固体.
【提出问题】白色固体含有什么物质?
【猜想与假设】
小李猜:白色固体含有Na2CO3;
小刚猜:白色固体含有Na2O;
小芳猜:白色固体含有NaOH.
【实验验证】
小李和小刚一致认为小芳的猜想不成立,他们的理由是反应物中不含有氢元素,一定不能生成氢氧化钠.
【反思提高】Na在CO2中燃烧存在多个反应、生成多种物质.请你写出其中生成物仅为一种白色固体与一种黑色固体的反应的化学方程式:3CO2+4Na$\frac{\underline{\;点燃\;}}{\;}$2Na2CO3+C.
【拓展应用】K、Ca、Na等活泼金属发生的火灾不能用二氧化碳灭火器灭火,你的理由是二氧化碳能够支持这些物质燃烧.
 某化学课外兴趣小组为探究Na与CO2的反应进行了如下实验(实验部分装置如图所示):向盛有Na的装置A中通入纯净、干燥的CO2,当观察到装置B中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,Na剧烈燃烧,产生白烟,燃烧结束后装置A中有黑色固体和白色固体生成.
某化学课外兴趣小组为探究Na与CO2的反应进行了如下实验(实验部分装置如图所示):向盛有Na的装置A中通入纯净、干燥的CO2,当观察到装置B中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,Na剧烈燃烧,产生白烟,燃烧结束后装置A中有黑色固体和白色固体生成.【资料卡】
(1)K、Ca、Na等活泼金属的氧化物均可与水反应生成对应的碱;
(2)钠为银白色金属,过氧化钠为淡黄色固体.
【提出问题】白色固体含有什么物质?
【猜想与假设】
小李猜:白色固体含有Na2CO3;
小刚猜:白色固体含有Na2O;
小芳猜:白色固体含有NaOH.
【实验验证】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量白色固体放入足量水中 | 白色固体完全溶解 | / |
| ②取①中少量溶液,加入稀盐酸 | 产生大量气泡 | 小李的猜想成立 |
| ③取①中少量溶液,加入足量CaCl2溶液,待沉淀完全后,加入2~3滴酚酞试液 | 酚酞试液变红色 | 小刚的猜想成立 |
【反思提高】Na在CO2中燃烧存在多个反应、生成多种物质.请你写出其中生成物仅为一种白色固体与一种黑色固体的反应的化学方程式:3CO2+4Na$\frac{\underline{\;点燃\;}}{\;}$2Na2CO3+C.
【拓展应用】K、Ca、Na等活泼金属发生的火灾不能用二氧化碳灭火器灭火,你的理由是二氧化碳能够支持这些物质燃烧.
16.生活中常见的下列变化中,一定发生化学变化的是( )
| A. | 葡萄酿酒 | B. | 西瓜榨汁 | C. | 水结成冰 | D. | 酒精挥发 |
6.下列设计的实验方案中不能达到目的是( )
| A. | 除去粗盐中的泥沙,采用溶解、过滤、蒸发的步骤 | |
| B. | 用MnO2来区分水和过氧化氢溶液 | |
| C. | 用稀盐酸除去铁粉中混有的少量铜粉 | |
| D. | 用Ba(OH)2溶液检验露置在空气中的NaOH溶液是否变质 |
13.碳酸钠(Na2CO3)和碳酸氢钠(NaHCO3)为常见的两种化合物,其中碳酸钠最为重要,在工业上有广泛的应用.在生活中,碳酸氢钠是常用的发酵剂的主要成分.
Ⅰ.(1)碳酸钠和碳酸氢钠中阴离子对应的酸都是H2CO3(填化学式)
(2)碳酸氢钠在医疗上用作治疗胃酸过多,反应的化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑.
Ⅱ.某天然碱中可能含有碳酸钠和碳酸氢钠,小明同学设计了如下实验探究其组成.请分析其过程完成填空.
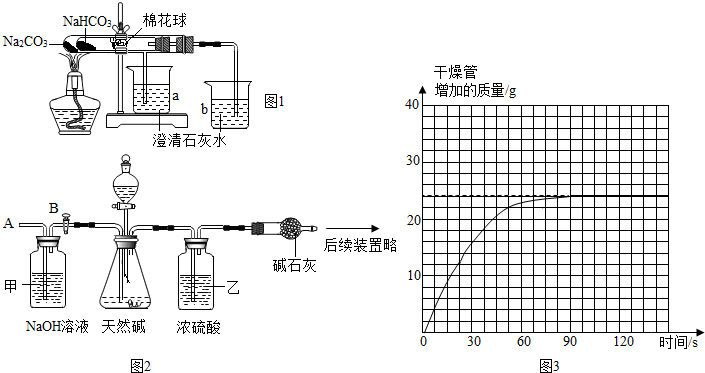
在老师的指导下采用了图1所示装置用小苏打和纯碱做了对比实验.实验中小试管内沾有无水硫酸铜粉末的棉花球变成蓝色,a烧杯中石灰水无明显现象,b烧杯中石灰水了现白色浑浊.试回答:①结论:碳酸氢钠(填“碳酸钠”或“碳酸氢钠”)受热分解出水和CO2等物质;②写出b烧杯中发生反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
同学们还查阅到如下资料:
(1)2NaHCO3+Ca(OH)2=Na2CO3+CaCO3↓+H2O
(2)Ca(HCO3)2+Na2CO3=CaCO3↓+2NaHCO3
(3)CaCl2稀溶液与NaHCO3稀溶液混合无沉淀、与Na2CO3稀溶液混合有沉淀
【假设猜想】
假设一:天然碱成分为碳酸氢钠;
假设二:天然碱成分为碳酸钠;
假设三:天然碱成分为碳酸氢钠和碳酸钠.
【实验方案】
方案一:取一定量样品直接加热,再将产生的气体通入澄清石灰水,根据实验现象,对上述三种假设的每一种是否成立都能进行判断.请评价这种方案是否合理否(填“是”或“否”),理由是只能得出是否含有碳酸氢钠或碳酸钠,不能判断是否同时含有碳酸氢钠和碳酸钠.
方案二:
可选药品:NaOH溶液 稀盐酸 Ca(OH)2溶液 CaCl2溶液
Ⅲ.为测定天然碱中的成分,小组的同学设计了如下实验,其主要实验步骤如下:
(1)按图组装仪器,将52.5g试样放入锥形瓶中,打开活塞B,从导管A处缓缓鼓入一定量的空气;
(2)准确称量干燥管的质量后再次连接好装置;
(3)关闭活塞B,打开分液漏斗的活塞和上面的塞子,加入足量某酸溶液;
(4)待锥形瓶中不再产生气泡时,打开活塞B,再次从导管A处缓缓鼓入一定量的空气,直至干燥管内物质质量不变;
(5)再次称量干燥管的质量;并绘制干燥管增加的质量与时间的关系图2、图3(见图);
讨论:
①步骤(1)加入样品前还应检查装置的气密性,所加的酸溶液最好是稀硫酸.
②装置甲的作用是吸收空气中的二氧化碳;装置乙的作用是吸收二氧化碳中混有的水蒸气.第(4)步再次从导管A处缓缓鼓入一定量的空气的作用是使反应生成的二氧化碳全部被碱石灰吸收.
③请利用有关数据计算试样中碳酸氢钠的质量分数.(写出计算过程)
Ⅰ.(1)碳酸钠和碳酸氢钠中阴离子对应的酸都是H2CO3(填化学式)
(2)碳酸氢钠在医疗上用作治疗胃酸过多,反应的化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑.
Ⅱ.某天然碱中可能含有碳酸钠和碳酸氢钠,小明同学设计了如下实验探究其组成.请分析其过程完成填空.

在老师的指导下采用了图1所示装置用小苏打和纯碱做了对比实验.实验中小试管内沾有无水硫酸铜粉末的棉花球变成蓝色,a烧杯中石灰水无明显现象,b烧杯中石灰水了现白色浑浊.试回答:①结论:碳酸氢钠(填“碳酸钠”或“碳酸氢钠”)受热分解出水和CO2等物质;②写出b烧杯中发生反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
同学们还查阅到如下资料:
(1)2NaHCO3+Ca(OH)2=Na2CO3+CaCO3↓+H2O
(2)Ca(HCO3)2+Na2CO3=CaCO3↓+2NaHCO3
(3)CaCl2稀溶液与NaHCO3稀溶液混合无沉淀、与Na2CO3稀溶液混合有沉淀
【假设猜想】
假设一:天然碱成分为碳酸氢钠;
假设二:天然碱成分为碳酸钠;
假设三:天然碱成分为碳酸氢钠和碳酸钠.
【实验方案】
方案一:取一定量样品直接加热,再将产生的气体通入澄清石灰水,根据实验现象,对上述三种假设的每一种是否成立都能进行判断.请评价这种方案是否合理否(填“是”或“否”),理由是只能得出是否含有碳酸氢钠或碳酸钠,不能判断是否同时含有碳酸氢钠和碳酸钠.
方案二:
可选药品:NaOH溶液 稀盐酸 Ca(OH)2溶液 CaCl2溶液
| 实验操作 | 实验现象 | 实验结论 |
| 操作一:取天然碱样品少量溶于足量水后,加入过量的CaCl2稀溶液(如果操作一有沉淀,则进行操作二) | 无沉淀出现 | 假设一成立 |
| 操作二:待操作一中反应充分后过滤,并在滤液中加入过量的Ca(OH)2溶液,观察. | 无沉淀出现 | 假设二成立 |
| 产生白色沉淀 | 假设三成立 |
(1)按图组装仪器,将52.5g试样放入锥形瓶中,打开活塞B,从导管A处缓缓鼓入一定量的空气;
(2)准确称量干燥管的质量后再次连接好装置;
(3)关闭活塞B,打开分液漏斗的活塞和上面的塞子,加入足量某酸溶液;
(4)待锥形瓶中不再产生气泡时,打开活塞B,再次从导管A处缓缓鼓入一定量的空气,直至干燥管内物质质量不变;
(5)再次称量干燥管的质量;并绘制干燥管增加的质量与时间的关系图2、图3(见图);
讨论:
①步骤(1)加入样品前还应检查装置的气密性,所加的酸溶液最好是稀硫酸.
②装置甲的作用是吸收空气中的二氧化碳;装置乙的作用是吸收二氧化碳中混有的水蒸气.第(4)步再次从导管A处缓缓鼓入一定量的空气的作用是使反应生成的二氧化碳全部被碱石灰吸收.
③请利用有关数据计算试样中碳酸氢钠的质量分数.(写出计算过程)
10.下列物质在氧气中燃烧,生成黑色固体的是( )
| A. | 木炭 | B. | 铁丝 | C. | 硫粉 | D. | 红磷 |