��Ŀ����
3���ڲⶨһƿ�Ȼ��ƺ�̼���ƻ����ʱ��������ʵ�飮
��ش��������⣺
��1��ʵ���з�����Ӧ�Ļ�ѧ����ʽ��Na2CO3+CaCl2�TCaCO3��+2NaCl��
��2����������з�����Ӧ������������X���ı���ʽ��$\frac{106}{x}=\frac{100}{10g}$��
��3����������Ȼ��ƺ�̼���������������������22��53��
��4��ʵ��ʱ�����������ܼ���ʧ����������Һ����15gˮ������������������ʱ������Һ�����ʵ�����������16.1%��
���� ��1����ʵ��̼�������Ȼ��Ʒ�Ӧ����̼��Ƴ������Ȼ��ƣ����������غ㶨����ȷ��д��ѧ����ʽ��
��2�����ݻ�ѧ����ʽ�и����ʵ������ȷ������
��3�����ݻ�ѧ����ʽ����ϳ����������������̼���Ƶ��������ɽ��
��4���������ʵ�����������ʽ������
��� �⣺��1����ʵ��̼�������Ȼ��Ʒ�Ӧ����̼��Ƴ������Ȼ��ƣ���ѧ����ʽΪ��Na2CO3+CaCl2=CaCO3��+2NaCl��
��2����̼���Ƶ�����Ϊx�������Ȼ��Ƶ�����Ϊy��
Na2CO3+CaCl2=CaCO3��+2NaCl
106 100 117
x 10g y
$\frac{106}{x}=\frac{100}{10g}$��
x=10.6g
$\frac{100}{10g}=\frac{117}{y}$
y=11.7g
��3����������Ȼ��ƺ�̼������������������ȣ���15g-10.6g����10.6g=22��53��
��4��������Һ�����ʵ����������ǣ�$\frac{11.7g+��15g-10.6g��}{15g+50g+60g-10g-15g}��100%$=16.1%��
�ʴ�Ϊ����1��Na2CO3+CaCl2�TCaCO3��+2NaCl��
��2��$\frac{106}{x}=\frac{100}{10g}$����3��22��53����4��16.1%��
���� ���⿼�����Ȼ�����̼���ƵĻ�ѧ���ʣ�ͬʱ�����˻�ѧ����ʽ����д�Լ����ݻ�ѧ����ʽ������Һ������������Ҫ��ѧ���������ճ������ʵĻ�ѧ�����Լ���صĻ�ѧ����ʽ��

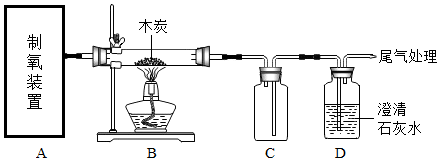
| A�� | ���ڴ��� | B�� | ����ʯ���� | C�� | �������� | D�� | ���ܵ� |
| A�� | ͭ˿�������� | B�� | ���������������� | ||
| C�� | ������������ȥ������ | D�� | þ�������̻��������� |
| A�� | ������̼ | B�� | ����������� | C�� | ϡ������ | D�� | ���� |
ʳƷ���Ӽ�
ʳƷ���Ӽ�ָ������ʳƷ�Ĺ����У���ʳƷ�м���Ļ�ѧ���ʣ�
ʳƷ���Ӽ�һ�㲻������ΪʳƷ��ʳ�ã�����������Ȼ���ʣ�Ҳ�������˹��ϳɵ����ʣ��������뵽ʳƷ����Ϊ�˸���ʳƷ��ɫ���㡢ζ��ͬʱҲ�����������ʵ����ã�
��ĿǰΪֹ��ȫ����ʳƷ���Ӽ�Ʒ�ִﵽ25000�֣����Ƕ�����ʳ�ã����ǣ��������谷����ȸʯ�̡��յ��������ȴ��ֹ��ʳƷ�����ӣ���Ϊ�����ǻ���ԭ�ϣ�
�ҹ���ʳƷ���Ӽ�ʹ�����������й涨�˸���ʳƷ��ʳƷ���Ӽ��İ�ȫ����������Ϊ��ζ���ġ������ء�����ʹ�÷�Χ�����ʹ�������±���ʾ��
| ʹ�÷�Χ | ���ʹ������g/kg�� |
| ���ˡ���ζ��֭����㡢����ܡ����ϵ� | 0.65 |
| �۽� | 1.0 |
| ��Ƥ����÷�������÷�ɵ� | 8.0 |
Ŀǰ��97%��ʳƷ��ʹ���˸������Ӽ�������˵��ʳƷ���Ӽ��ѳ�Ϊ�ִ�ʳƷ��ҵ�����в���ȱ�ٵ����ʣ�
��1���յ��첻�ǣ���ǡ����ǡ���ʳƷ���Ӽ���
��2��ij���Ա��100gijƷ�ƻ�÷�м���1.01g�������أ��жϸû�÷���������Ƿ곬�꣮
��3�����������غ����ǵķ����Ƿֱ�ȡ�����м��ȣ����ۻ�����ڵ������ǣ�������������������أ�
��4�����й���ѡ��ʳƷ������ȷ����BC��
A��ֻѡ��ʳƷ���Ӽ���ʳƷ
B����עʳƷӪ���������Ӽ���Ʒ�ֺ�����
C��ѡ��ӹ��ȵ͵�ʳƷ�����������������Ӽ�
D��ֻ��עʳƷ��Ӫ���ɷ֣����ں��Ƿ������Ӽ�
��5�������Ƿ���ҪʳƷ���Ӽ���˵�����ɣ�ʳƷ���Ӽ����뵽ʳƷ�л����ʳƷ��ɫ���㡢ζ��ͬʱҲ�����������ʵ����ã���ֻҪ������ʹ�ã�����Ӱ�����彡����
 �ҹ���һ��������ƺͽ���ĺ�ĸ�Ѿ���װ���ṹװ�ޣ���ϣ�����ʹ���������²��Ϻ��¼�����
�ҹ���һ��������ƺͽ���ĺ�ĸ�Ѿ���װ���ṹװ�ޣ���ϣ�����ʹ���������²��Ϻ��¼�����