题目内容
9. 向盛有一定质量稀硫酸的烧杯中逐渐加入10g锌粒,产生气体质量与锌粒质量的关系如图所示;充分反应后,称得烧杯中剩余物质总质量为109.8g.请根据关系图分析并计算:
向盛有一定质量稀硫酸的烧杯中逐渐加入10g锌粒,产生气体质量与锌粒质量的关系如图所示;充分反应后,称得烧杯中剩余物质总质量为109.8g.请根据关系图分析并计算:(1)稀硫酸反应完时,产生氢气的质量为0.2g,消耗锌粒质量为6.5g.
(2)该稀硫酸中溶质的质量(写出计算过程).
分析 锌和稀硫酸反应生成硫酸锌和氢气,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)由图中数据可知,稀硫酸反应完时,产生氢气的质量为0.2g;
(2)设消耗锌粒质量为x,反应的硫酸质量为y,
Zn+H2SO4═ZnSO4+H2↑,
65 98 2
x y 0.2g
$\frac{65}{x}$=$\frac{98}{y}$=$\frac{2}{0.2g}$,
x=6.5g,y=9.8g,
故答案为:0.2;6.5;硫酸中溶质的质量为9.8g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.规范操作是实验成功的保证,下列实验操作中正确的是( )
| A. |  闻气体的气味 | B. |  像试管里加粉末 | C. |  点燃酒精灯 | D. |  滴加液体 |
20.下列课外小实验不涉及化学变化的是( )
| A. | 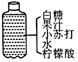 自制汽水 | B. | 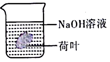 叶脉书签制作 | C. | 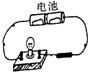 验证石墨导电性 | D. |  食醋去除水垢 |
17.下列化学方程式符合题意且书写正确的是( )
| A. | 用盐酸除铁锈:Fe2O3+6HCl=2FeCl2+3H2O | |
| B. | 铁与盐酸反应:2Fe+6HCl=2FeCl3+3H2↑ | |
| C. | 制取少量硫酸镁:MgCl2+Na2SO4=MgSO4+2NaCl | |
| D. | 吸收二氧化硫气体:SO2+2NaOH=Na2SO3+H2O |
18.下列关于溶液的说法中正确的是( )
| A. | 溶液的特点是均一稳定,无色透明 | |
| B. | 继续往溶液中增加溶质,溶质还能溶解,说明原溶液已经饱和 | |
| C. | 饱和溶液一定是非常浓的溶液,不饱和溶液一定是非常稀的溶液 | |
| D. | 溶液加水稀释前后溶质的质量不变 |