题目内容
 酸、碱、盐是几类重要的化合物,他们之间能发生复分解反应.
酸、碱、盐是几类重要的化合物,他们之间能发生复分解反应.(1)浓硫酸具有吸水性,在实验室中常用它做
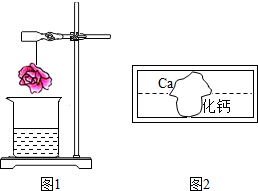
(2)如图1,用滤纸做成的小花喷洒某溶液后放在烧杯上方,片刻后变成红
色,请推测喷洒液和烧杯中溶液可能是什么?(写出一组即可)
(3)工业上常用稀盐酸来除铁锈,写出反应化学反应方程式
(4)粗盐水中主要含有Ca2+、Mg 2+、SO42-等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂的合理的顺序为
| OH- | SO42- | CO32- | |
| Ba2+ | 溶 | 不溶 | 不溶 |
| Ca2+ | 微溶 | 微溶 | 不溶 |
| Mg2+ | 不溶 | 溶 | 微溶 |
| 实验操作 | 实验现象 | 实验结论 |
| 取少伙”溶液于试管中.向其中滴加 | 猜想①正确 |
考点:浓硫酸的性质及浓硫酸的稀释,缺失标签的药品成分的探究,一定溶质质量分数的溶液的配制,酸碱指示剂及其性质,酸的化学性质,氯化钠与粗盐提纯,根据化学反应方程式的计算
专题:有关化学方程式的计算,常见的酸 酸的通性,常见的盐 化学肥料,科学探究
分析:(1)根据物质的性质进行分析,浓硫酸具有吸水性,常用于干燥剂;
(2)滤纸做成的小花喷上某溶液后放在烧杯上方,片刻后变成红色;根据紫色石蕊溶液遇酸性溶液变红色,无色酚酞溶液遇碱性溶液变红色,结合常见的具有挥发性的溶液进行分析解答.
(3)铁锈的主要成分是氧化铁,它能与稀盐酸反应生成氯化铁和水;配制溶液所需要的仪器主要有量筒、烧杯、玻璃棒、胶头滴管;
(4)根据加入碳酸钠的两个作用考虑加入试剂的顺序;
(5)根据碳酸钠的性质和部分标签的内容进行猜想;根据氢氧化钙或氯化钙溶液的酸碱性分析设计实验;
(6)洗涤后溶液呈中性说明恰好完全反应,根据反应的化学方程式,由反应所消耗的氢氧化钠的质量计算出石油产品中硫酸的质量.
(2)滤纸做成的小花喷上某溶液后放在烧杯上方,片刻后变成红色;根据紫色石蕊溶液遇酸性溶液变红色,无色酚酞溶液遇碱性溶液变红色,结合常见的具有挥发性的溶液进行分析解答.
(3)铁锈的主要成分是氧化铁,它能与稀盐酸反应生成氯化铁和水;配制溶液所需要的仪器主要有量筒、烧杯、玻璃棒、胶头滴管;
(4)根据加入碳酸钠的两个作用考虑加入试剂的顺序;
(5)根据碳酸钠的性质和部分标签的内容进行猜想;根据氢氧化钙或氯化钙溶液的酸碱性分析设计实验;
(6)洗涤后溶液呈中性说明恰好完全反应,根据反应的化学方程式,由反应所消耗的氢氧化钠的质量计算出石油产品中硫酸的质量.
解答:解:(1)浓硫酸具有吸水性,常用作某些气体的干燥剂.故填:干燥剂;
(2)滤纸做成的小花喷上某溶液后放在烧杯上方,片刻后变成红色;
若喷洒的是石蕊溶液,则烧杯中的应是具有挥发性的酸性溶液,浓盐酸具有挥发性,挥发出来的氯化氢气体溶于水生成盐酸使紫色石蕊溶液变红色;
若喷洒的是酚酞溶液,则烧杯中的应是具有挥发性的碱性溶液,浓氨水有挥发性,挥发出的氨气体遇到试剂中的水形成氨水,氨水呈碱性,无色的酚酞溶液遇碱性溶液变红色.
综上所述,喷洒液和烧杯中溶液可能是石蕊溶液和浓盐酸(或酚酞溶液和浓氨水).
(3)铁锈的主要成分是氧化铁,它能与稀盐酸反应生成氯化铁和水,反应方程式Fe2O3+6HCl═2FeCl3+3H2O;配制溶液所需要的仪器主要有量筒、烧杯、玻璃棒、胶头滴管;
故填:Fe2O3+6HCl═2FeCl3+3H2O;量筒、烧杯、玻璃棒、胶头滴管;
(4)加入碳酸钠的作用有两个:一个是除去溶液中的Ca2+、另一个是除去过量的氯化钡,所以加入的碳酸钠必须排在氯化钡的后面,所以顺序是NaOH、BaCl2、Na2CO3;
故填:NaOH溶液、BaCl2溶液、Na2CO3溶液;
(5)①有标签可知,溶液为钙的化合物溶液,能与碳酸钠的反应可能是氢氧化钙或氯化钙;
②由于氢氧化钙溶液显碱性,氯化钙溶液呈中性,所以,设计实验如下;
故填:氢氧化钙;酚酞;溶液变红;
(6)设一定量石油产品中硫酸的质量为x
2NaOH+H2SO4═Na2SO4+2H2O
80 98
40g×15% x
=
x=7.35g
答:此一定量的石油产品里硫酸的质量是7.35g.
(2)滤纸做成的小花喷上某溶液后放在烧杯上方,片刻后变成红色;
若喷洒的是石蕊溶液,则烧杯中的应是具有挥发性的酸性溶液,浓盐酸具有挥发性,挥发出来的氯化氢气体溶于水生成盐酸使紫色石蕊溶液变红色;
若喷洒的是酚酞溶液,则烧杯中的应是具有挥发性的碱性溶液,浓氨水有挥发性,挥发出的氨气体遇到试剂中的水形成氨水,氨水呈碱性,无色的酚酞溶液遇碱性溶液变红色.
综上所述,喷洒液和烧杯中溶液可能是石蕊溶液和浓盐酸(或酚酞溶液和浓氨水).
(3)铁锈的主要成分是氧化铁,它能与稀盐酸反应生成氯化铁和水,反应方程式Fe2O3+6HCl═2FeCl3+3H2O;配制溶液所需要的仪器主要有量筒、烧杯、玻璃棒、胶头滴管;
故填:Fe2O3+6HCl═2FeCl3+3H2O;量筒、烧杯、玻璃棒、胶头滴管;
(4)加入碳酸钠的作用有两个:一个是除去溶液中的Ca2+、另一个是除去过量的氯化钡,所以加入的碳酸钠必须排在氯化钡的后面,所以顺序是NaOH、BaCl2、Na2CO3;
故填:NaOH溶液、BaCl2溶液、Na2CO3溶液;
(5)①有标签可知,溶液为钙的化合物溶液,能与碳酸钠的反应可能是氢氧化钙或氯化钙;
②由于氢氧化钙溶液显碱性,氯化钙溶液呈中性,所以,设计实验如下;
| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于试管中,向其中滴加酚酞 | 溶液变红 | 猜想①正确, |
(6)设一定量石油产品中硫酸的质量为x
2NaOH+H2SO4═Na2SO4+2H2O
80 98
40g×15% x
| 80 |
| 40g×15% |
| 98 |
| x |
答:此一定量的石油产品里硫酸的质量是7.35g.
点评:根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列叙述正确的是( )
| A、纯净物中只含有一个分子 |
| B、某种物质中含有氧元素和另一种元素,则该物质一定是氧化物 |
| C、某种物质不是化合物就是单质 |
| D、某纯净物不是单质就是化合物 |
下列关于元素的叙述中,错误的是( )
| A、同种元素的质子数一定相同 |
| B、元素是具有相同核电荷数的一类原子的总称 |
| C、同种元素的中子数不一定相同 |
| D、同种元素的质子数一定等于中子数 |
下列关于氧气性质的叙述,正确的是( )
| A、氧气的密度比空气略大 |
| B、氧气有可燃性,是一种常用的燃料 |
| C、氧气易溶解于水 |
| D、化学性质很活泼,能与所有的物质发生反应 |
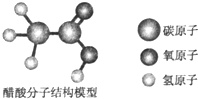 食醋是厨房中的一种调味品,其中含有少量醋酸.醋酸分子的结构模型如图所示:
食醋是厨房中的一种调味品,其中含有少量醋酸.醋酸分子的结构模型如图所示: