题目内容
 某兴趣小组的同学在化学实验室中制取氧气,如图.他们将氯酸钾和二氧化锰的混合物32.5g加热,充分反应,待试管冷却后称量试管内物质质量为22.9g.请计算(假设实验过程中无物质的损耗):
某兴趣小组的同学在化学实验室中制取氧气,如图.他们将氯酸钾和二氧化锰的混合物32.5g加热,充分反应,待试管冷却后称量试管内物质质量为22.9g.请计算(假设实验过程中无物质的损耗):(1)同学们可收集到多少克氧气?
(2)反应物中氯酸钾有多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:氯酸钾在二氧化锰的催化作用下分解生成氯化钾和氧气,反应前后的质量差即为反应生成氧气的质量,根据氧气的质量可以计算氯酸钾的质量.
解答:解:(1)根据质量守恒定律可知生成氧气的质量为:32.5g-22.9g=9.6g,
答:生成了9.6g氧气.
(2)设:反应物中氯酸钾的质量为x,
2KClO3
2KCl+3O2↑,
245 96
x 9.6g
245:96=x:9.6g,
x=24.5g,
答:反应物中氯酸钾的质量为24.5g.
答:生成了9.6g氧气.
(2)设:反应物中氯酸钾的质量为x,
2KClO3
| ||
| △ |
245 96
x 9.6g
245:96=x:9.6g,
x=24.5g,
答:反应物中氯酸钾的质量为24.5g.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组物质的稀溶液中,不用其他试剂就能鉴别出来的是( )
| A、Na2CO3、HCl、CaCl2、HNO3 |
| B、CaCl2、NaOH、Na2CO3、HCl |
| C、NH4Cl、KOH、Na2SO4、BaCl2 |
| D、FeCl3、HCl、NaOH、HNO3 |
人们在工作、生活中,为防止事故发生常采用一些安全措施,下列安全措施中正确的是( )
| A、高层着火开窗通风 |
| B、冬天用煤取暖时保证通风良好 |
| C、到煤窖中挖煤用火把照明 |
| D、厨房内煤气泄漏打开排气扇通风 |
控制变量法是实验探究的重要方法,下列设计方案中探究目的不能实现的是( )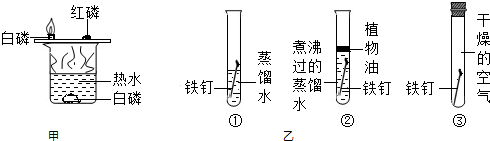

| A、甲实验可探究可燃物的燃烧需要与氧气接触且温度达到着火点 |
| B、甲实验中a、b对比可探究可燃物的燃烧是否需要达到一定温度 |
| C、乙中①②③对比可探究铁的锈蚀条件与氧气和水等物质是否有关 |
| D、乙中①③对比可探究铁的锈蚀条件与氧气是否有关 |
推理是化学学习的一种重要方法.下列推理关系合理的是( )
| A、原子团作为一个整体参加反应,所以原子团在任何反应中都不可拆分 |
| B、某物质燃烧生成二氧化碳和水,该物质中一定含有碳、氢、氧三种元素 |
| C、氧化汞受热分解生成汞和氧气,所以氧化汞由汞元素和氧元素组成 |
| D、纸张燃烧后余烬的质量比原纸张的质量小,所以该反应不符合质量守恒定律 |
下列微粒符号中,对“2”的含义理解正确的是( )
| A、2Mg表示2个镁元素 |
| B、2CO表示2个一氧化碳分子 |
| C、Zn2+表示Zn的化合价为+2价 |
| D、H2表示2个两个氦原子 |
水是一种重要的自然资源,与生物生存、工农业生产等息息相关.下列有关水的认识或观点错误的是( )
| A、尽管水分子很小,但它是由更小的微粒构成的 |
| B、在淡水资源缺乏的海岛上,可以用蒸馏法从海水中提取淡水 |
| C、水是由氢气和氧气组成的一种氧化物 |
| D、水是良好的溶剂,许多物质都能溶于水 |
 如图为A~E物质之间的转化关系,部分转化条件未标出.已知:A为黑色固体单质,B为红色粉末,A、D形成的合金是生产、生活中使用最多的金属材料,甲为常见的气体单质.请按要求完成下列空白:
如图为A~E物质之间的转化关系,部分转化条件未标出.已知:A为黑色固体单质,B为红色粉末,A、D形成的合金是生产、生活中使用最多的金属材料,甲为常见的气体单质.请按要求完成下列空白: 如图所示,在250mL干燥的圆底烧瓶中,充满NH3,并用带尖嘴导管的单孔塞塞紧(导管另一端的橡胶管先用夹子夹紧).实验开始时,先将注射器中的水推入烧瓶中,一段时间后,打开夹子,会观察到
如图所示,在250mL干燥的圆底烧瓶中,充满NH3,并用带尖嘴导管的单孔塞塞紧(导管另一端的橡胶管先用夹子夹紧).实验开始时,先将注射器中的水推入烧瓶中,一段时间后,打开夹子,会观察到