题目内容
3.某兴趣小组在实验中模拟炼铁化学原理的实验,对固体产物成分等进行探究.【设计实验】
用一氧化碳还原纯净的氧化铁粉末,实验装置如图.
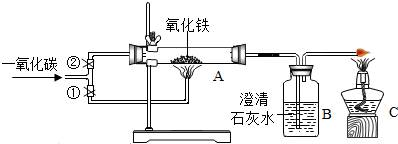
【进行实验】
(1)实验开始时,应先打开弹簧夹②(填“①”或“②”).
(2)C处点燃酒精灯的目的是点燃一氧化碳,防止污染空气.
【分析与讨论】
实验结束后,玻璃管内固体粉末由红棕色全部变成黑色,小明认为该黑色固体全部是单质铁,但小华提出了质疑,认为还可能是其它物质,如铁的常见氧化物:氧化铁、四氧化三铁、氧化亚铁(填名称).
【查阅资料】
上述氧化物中:氧化铁为红棕色,其余都为黑色;只有四氧化三铁能被磁铁吸引.
【实验与猜想】
(1)该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引.
(2)进行猜想:黑色固体粉末可能a.全部为铁 b.全部为四氧化三铁 c.铁和四氧化三铁
(3)该小组按上述猜想设计实验,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量m g(冷却到室温称量)
【得出结论】
通过实验中获得的数据进行计算:
(1)若猜想a成立,则m=64.2;
(2)若猜想b成立,反应的化学方程式为)CO+3Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe3O4+CO2;
(3)若猜想c成立,则m的取值范围为:64.2<m<65.8.
分析 【进行实验】(1)一氧化碳具有可燃性,实验开始要先通一会一氧化碳排尽试管内空气,防止一氧化碳与空气混合发生爆炸,;
(2)一氧化碳有毒,要进行尾气处理;
【实验与猜想】
(2)由于铁与四氧化三铁均能被磁铁吸引,所以可对黑色固体进行猜测;
【得出结论】依据实验测得的数据结合氧化铁的化学式可求出氧化铁中氧的质量,再用反应前后物质的质量差与之比较判断即可.
解答 解:
【进行实验】(1)一氧化碳具有可燃性,实验开始要先通一会一氧化碳排尽试管内空气,防止一氧化碳与空气混合发生爆炸,;
(2)一氧化碳有毒,要进行尾气处理;
【实验与猜想】
(2)由于铁与四氧化三铁均能被磁铁吸引,所以可对黑色固体的成分可能是:全部是铁;全部是四氧化三铁;两者的混合物;
【得出结论】依据实验测得的数据可知氧化铁的质量是:66g-60g=6g,这些氧化铁中含有的铁元素质量是:6g×$\frac{56×2}{56×2+16×3}×$100%=4.2g,由于反应前后元素的质量不变,所以若黑色粉末全部是铁,则反应后玻璃管和内盛黑色固体的总质量=60g+4.2g=64.2g;
假设全是四氧化三铁,根据其反应方程式可计算出生成的四氧化三铁的质量,设生成的四氧化三铁质量是x
CO+3Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe3O4+CO2
3×160 2×232
6g x
$\frac{3×160}{6g}=\frac{2×232}{x}$解得 x=5.8g
故若全部是四氧化三铁,反应后玻璃管和内盛黑色固体的总质量m=65.8g
若猜想c成立,则m的取值范围为64.2<m<65.8.
答案:
【进行实验】
(1)②
(2)点燃一氧化碳,防止污染空气
【分析与讨论】氧化亚铁
【实验与猜想】
(2)铁和四氧化三铁
【得出结论】(1)64.2 (2)CO+3Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe3O4+CO2 (3)64.2<m<65.8
点评 本题综合性较强,较全面的考查了一氧化碳还原氧化铁,尤其是利用数据对混合物的判断增加了试题难度,掌握反应前后元素的质量不变,并会结合方程式分析即可顺利解答.

 阅读快车系列答案
阅读快车系列答案| A. | 2:1 | B. | 9:8 | C. | 3:2 | D. | 4:7 |
| A. | ①③⑤ | B. | ②③⑤ | C. | ②③④ | D. | ①④⑤ |
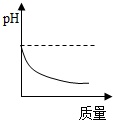 下列操作过程中,溶液pH随加入物质质量变化与如图所示相符的是( )
下列操作过程中,溶液pH随加入物质质量变化与如图所示相符的是( )| A. | 向稀硫酸中逐滴加入氢氧化钠溶液 | B. | 向氢氧化钠溶液中逐滴加水稀释 | ||
| C. | 向水中不断通入氯化氢气体 | D. | 向稀盐酸中加入石灰石 |
| A. | 高粱酿酒、呼吸作用 | B. | 石灰水变浑浊、石油分馏 | ||
| C. | 锅炉爆炸、白磷自燃 | D. | 水的电解、干冰升华 |
| A. |  | B. |  | C. |  | D. |  |

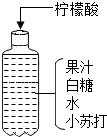 我县某课外活动小组按如图配方自做一瓶清凉甘甜的汽水,根据图中信息回答:
我县某课外活动小组按如图配方自做一瓶清凉甘甜的汽水,根据图中信息回答: