题目内容
10.有一包白色固体,可能含有FeCl3、CaCO3、NaOH、Ba(OH)2、BaCl2、Na2SO4中的几种.为确定其组成,取适量试样进行下列实验.请根据实验现象判断:①取试样溶于水,搅拌、过滤,得到无色澄清溶液A和白色沉淀B;
②取上述无色澄清溶液A,通入适量的CO2,生成白色沉淀C;
③取上述白色沉淀B,加入过量的稀硝酸,沉淀全部消失.
综合上述实验现象,下列判断正确的是( )
| A. | 由①得原白色固体中一定不含FeCl3,一定含量有CaCO3 | |
| B. | 由②③得原白色固体中一定含有Ba(OH)2,一定不含量有Na2SO4 | |
| C. | 由实验现象判断,白色固体中至少有3种固体 | |
| D. | 由实验现象判断,白色固体的组成可有5种情况 |
分析 由于含Fe3+溶液呈黄色,其沉淀为红褐色,根据白色固体溶于水得到无色溶液A和白色沉淀B,可确定白色固体中不含FeCl3;
白色固体若只含两种物质,则根据(2)通入二氧化碳气体得到白色固沉淀,而在几种物质的溶液中,能与气体CO2反应形成沉淀的只有Ba(OH)2,也可以是NaOH、BaCl2或者NaOH、Ba(OH)2、BaCl2. 根据(3)中白色沉淀B全部溶于稀硝酸,可判断白色沉淀为CaCO3;确定不能存在硫酸钠.
解答 解:由于含Fe3+溶液呈黄色,其沉淀为红褐色,根据白色固体溶于水得到无色溶液A和白色沉淀B,可确定白色固体中不含FeCl3;
白色固体若只含两种物质,则根据(2)通入二氧化碳气体得到白色固沉淀,而在几种物质的溶液中,能与气体CO2反应形成沉淀的只有Ba(OH)2,也可以是NaOH、BaCl2或者NaOH、Ba(OH)2、BaCl2. 根据(3)中白色沉淀B全部溶于稀硝酸,可判断白色沉淀为CaCO3;确定不能存在硫酸钠.
白色固体若只含两种物质,则根据分析可以知道,固体A中一定含有CaCO3、Ba(OH)2,所以,若白色固体A中只含二种物质,它们是CaCO3、Ba(OH)2;
白色固体是由三种物质组成的,则白色固体A中一定含有CaCO3、Ba(OH)2或是氢氧化钠和氯化钡,一定不含FeCl3、Na2SO4,则白色固体含有三种物质,则可能的组成为:①CaCO3、Ba(OH)2、NaOH;②CaCO3、Ba(OH)2、BaCl2;③CaCO3、NaOH、BaCl2;
白色固体是由四种物质组成的,则白色固体A中一定含有CaCO3、Ba(OH)2、NaOH、BaCl2.
故选:D.
点评 根据物质的性质及变化规律,结合转化变化框图中的实验现象,确定固体中一定含有的物质与一定不含有的物质,然后对可能含有的物质进行组合.

 阅读快车系列答案
阅读快车系列答案| A. | 都含有氧元素 | B. | 都含氧分子 | C. | 都属于氧化物 | D. | 都是化合物 |
(1)石油、煤、天然气合称为三大化石燃料.
①煤燃烧时排放出SO2、NO2等污染物,这些气体或气体在空气中发生反应后的生成物溶于雨水会形成酸雨.
②2014年青奥会在南京举行,为了控制汽车尾气给空气造成的污染,我市在燃料的使用和管理等方面采取了一些有效措施,如节能环保车的使用,这也是未来的发展趋势.

图2是我国自行研制的氢动力概念跑车.汽车最理想的清洁燃料是氢气,但氢动力汽车目前还不能普及的原因是氢气制取成本高或贮存困难(只需写出一点).
(2)水是地球上最普通、最常见的物质之一.
①自来水厂净化水的步骤一般有加絮凝剂、沉淀、过滤、活性炭吸附、消毒剂消毒等步骤.检验自来水是否为硬水常用的物质是肥皂水.生活中通过煮沸的方法可以降低水的硬度.实验室配制氯化钠溶液应该用蒸馏水(填“自来水”或“蒸馏水”).
②从社会角度看:2014年3月22-28日是第二十七届“中国水周”.活动的宣传主题为“节约保护水资源,大力建设生态文明”.下列做法符合宣传主题的是AB.
A.富含氮、磷的生活污水不能排放到河中 B.农业浇灌推广使用喷灌、滴灌技术
C.不间断地放水洗衣服 D.工业污水直接压入地下
③新型自来水净水剂ClO2可由如下反应制取:Cl2+2X═2NaCl+2ClO2,X的化学式为NaClO2.
(3)人类每年都要从大自然中提取大量的金属,用于工农业生产和其他领域.
铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.
①用下列试剂验证这三种金属的活动性顺序,能达到目的是B(填序号).
A.硫酸铝溶液 B.硫酸亚铁溶液 C.硫酸铜溶液
②某工厂的废液中含有硝酸银和硝酸铜,为回收资源和防止污染,向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入稀盐酸,无气体产生.下列说法正确的是A(选填字母).
A.滤渣中一定含有银,可能含有铜
B.滤渣中一定含有银和铜,一定没有铁
C.滤液中一定含有硝酸亚铁,一定没有硝酸银
D.滤液中一定含有硝酸亚铁,一定没有硝酸铜
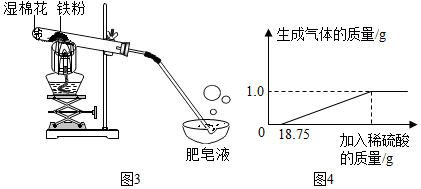
③常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
a.试管尾部放一团湿棉花的目的是提供水蒸气.
b.探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是H2.
c.探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是Fe3O4.
【实验探究】
| 实验操作 | 实验现象及结论 |
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3红棕色粉末且不能被磁铁吸引.
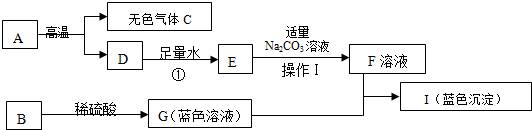
④某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅、锰等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应).兴趣小组的同学称取33g废铁锅片放入特制容器中,缓慢加入39.2%的稀硫酸,直到反应完全(假设硫酸先与表面的铁锈发生反应),实验数据如图4所示.所得溶液中所含溶质的化学式为Fe2(SO4)3、FeSO4,计算溶液中硫酸铁的质量.(要求写出计算过程)
| A. | 油锅着火用锅盖盖灭 | |
| B. | 睡觉时闻到很重的煤气味,打开电灯检查煤气罐漏气部位 | |
| C. | 室内起火时打开门窗通风 | |
| D. | 图书馆内图书起火,立即用泡沫灭火器扑灭 |
| A. | 一定是乙烧杯中产生的氢气多 | |
| B. | 可能是乙烧杯中产生的氢气多 | |
| C. | 一定是甲烧杯中产生的氢气多 | |
| D. | 可能甲、乙两烧杯中产生的氢气一样多 |
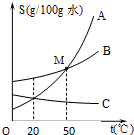 根据如图A、B、C三种固体的溶解度曲线回答:
根据如图A、B、C三种固体的溶解度曲线回答: