题目内容
15.实验室常用二氧化锰催化过过氧化氢溶液制取氧气,现将1 g二氧化锰放入盛有100g过氧化氢溶液的锥形瓶中.反应完全结朿后.称得锥形瓶内物质总质量为97.8g.计算:(1)反应生成的氧气的质量.
(2)计算原过氧化氢溶液中溶质的质量分数.
分析 (1)根据过氧化氢溶液和二氧化锰混合生成水和氧气,所以反应前后质量减少的就是氧气的质量;
(2)根据生成氧气的质量可以计算过氧化氢溶液中过氧化氢的质量.
解答 解:(1)过氧化氢溶液和二氧化锰混合生成水和氧气,所以反应前后质量减少的就是氧气的质量,所以氧气的质量=100g+1g-97.8g=3.2g;
答.反应生成的氧气的质量是3.2g
(2)设原过氧化氢溶液中过氧化氢的质量为x.
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 3.2g
$\frac{68}{x}=\frac{32}{3.2g}$
x=6.8g
原过氧化氢溶液中溶质的质量分数:$\frac{6.8g}{100g}×$100%=6.8%
答,原过氧化氢溶液中溶质的质量分数6.8%.
点评 催化剂在反应前后质量、化学性质都不变,而物理性质是否改变无法确定,理解催化剂的性质时要注意这一点.

练习册系列答案
相关题目
18.水是宝贵的自然资源,下列说法中正确的是( )
| A. | 水在自然界中循环,取之不尽,用之不竭 | |
| B. | 水是常见的溶剂,广泛用于工农业生产 | |
| C. | 为了节约用水,可以用工业废水直接浇灌农田 | |
| D. | 自来水中只含有水分子,是一种纯净物 |
6.随着人们对酒驾危害认识的加深,司法机关对于酒驾、醉驾的处罚将日趋加重.醉酒的原因是酒中含有的乙醇对人的神经系统有刺激作用.交警对呼气酒精检验的原理是:
白酒是乙醇的水溶液,酒中的乙醇在微生物作用下能被氧化成乙酸.小刚家有一瓶密封存放的白酒,他想知道该白酒的组成情况,于是进行如下实验探究:
【提出问题】该白酒中的溶质主要有哪些?
【查阅资料】
材料一:乙醇(C2H5OH),俗称酒精,易溶于水,水溶液呈中性.在加热条件下,可以把氧化铜还原为单质铜.
材料二:乙酸(CH3COOH),又名醋酸,易溶于水,具有酸的通性.
【提出猜想】
猜想1:只有乙醇
猜想2:只有乙酸
猜想3:乙醇和乙酸.
【实验探究】
【实验反思】
(1)操作①能否改为“将加热后的表面有黑色氧化铜的铜丝插入盛有白酒的试管中”?不能,理由是乙酸也能使铜丝表面由黑色变为红色.
(2)K2Cr2O7中铬元素的化合价为+6.
白酒是乙醇的水溶液,酒中的乙醇在微生物作用下能被氧化成乙酸.小刚家有一瓶密封存放的白酒,他想知道该白酒的组成情况,于是进行如下实验探究:
【提出问题】该白酒中的溶质主要有哪些?
【查阅资料】
材料一:乙醇(C2H5OH),俗称酒精,易溶于水,水溶液呈中性.在加热条件下,可以把氧化铜还原为单质铜.
材料二:乙酸(CH3COOH),又名醋酸,易溶于水,具有酸的通性.
【提出猜想】
猜想1:只有乙醇
猜想2:只有乙酸
猜想3:乙醇和乙酸.
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量白酒于试管中,滴入几滴橙色的K2Cr2O7酸性溶液 | 溶液变成蓝绿色 | 猜想1成立 |
| ②取少量白酒于试管中,滴入几滴紫色石蕊试液 | 石蕊试液不变色 |
(1)操作①能否改为“将加热后的表面有黑色氧化铜的铜丝插入盛有白酒的试管中”?不能,理由是乙酸也能使铜丝表面由黑色变为红色.
(2)K2Cr2O7中铬元素的化合价为+6.
3.下列属于化学变化的是( )
| A. | 酒精的挥发 | B. | 金属锈蚀 | C. | 车胎爆炸 | D. | 石蜡受热熔化 |
20.下列有关实验操作的“先”和“后”的说法中,正确的是( )
| A. | 若不慎将腐蚀性药液溅入眼睛,要先用手揉眼睛,后用水冲洗 | |
| B. | 给试管里的药品加热时,先均匀加热,后集中加热 | |
| C. | 用滴管取细口瓶内的液体时,先将其伸入液体内,后挤压取液 | |
| D. | 向试管中装入固体粉末时,先将试管直立,后把盛药品的药匙送至试管底部 |
4.下列图示的实验基本操作正确的是( )
| A. | 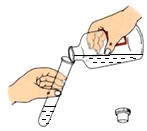 液体的取用 | B. | 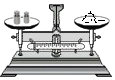 称取氯化钠 | C. | 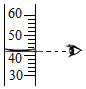 读取液体体积 | D. | 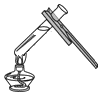 给液体加热 |
5.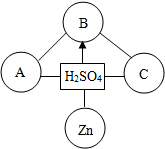 如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物,则A、B、C可能是( )
如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物,则A、B、C可能是( )
 如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物,则A、B、C可能是( )
如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物,则A、B、C可能是( )| A. | NaOH、CuSO4、Na2CO3 | B. | Ba(OH)2、CuCl2、CuO | ||
| C. | Cu(OH)2、HCl、Fe2O3 | D. | NaOH、HCl、Na2CO3 |