题目内容
16. 维生素C(简写成Vc)是人体必需的营养素,人体缺乏时易患坏血病.右图为某种维生索C片说明书的一部分,请回答下列问题.
维生素C(简写成Vc)是人体必需的营养素,人体缺乏时易患坏血病.右图为某种维生索C片说明书的一部分,请回答下列问题.(1)Vc中含有三种元素;
(2)Vc的相对分子质量是176,其中氢元素的质量分数是多少?(写出计算过程,结果精确到0.1%)
(3)如图所示的维生素C片,每片中含Vc0.051g;若成年人每天对Vc的
最低需要量为100mg,则:
①若Vc全部来自上图的维生素C片,每天至少服用2 片;
②若Vc全部来自某种新鲜蔬菜(每100g这种蔬菜含Vc 25mg),每天至少应食用这种蔬菜400g.
分析 (1)根据维生素C化学式的含义来分析;
(2)相对分子质量为构成分子的各原子的相对原子质量之和,化合物中某元素的质量分数来进行分析解答.
(3)分析和利用图示中提供的数据,首先求出每片钙片中含有的Vc,然后再去计算有关的量.
解答 解:(1)Vc是由碳元素、氢元素和氧元素三种元素组成的;故填:三;
(2)Vc的相对分子质量为12×6+1×8+16×6=176;其中氢元素的质量分数为:$\frac{8}{176}$×100%=4.5%;故填:176;4.5%.
(3)由标签可知,每片维生素C:0.85g中含有Vc6%,即每片维生素C中含Vc质量为:0.85g×6%=0.051g=51mg.故答案为:0.051.
若成年人每天最少补充100mgVc,而且①Vc完全由维生素C片补充,则每天至少服用$\frac{100mg}{51mg/片}$=2片,所以每次是2片.故答案为:2.
②若Vc完全由蔬菜来补充,则每天需要的蔬菜为$\frac{100mg}{25mg}$×100g=400g,故答案为:400.
点评 本题难度不大,考查同学们结合标签新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
6.下列说法正确的是( )
| A. | 木炭燃烧后生成红色固体 | B. | 硫在空气中燃烧发出蓝紫色火焰 | ||
| C. | 红磷在空气中燃烧产生大量白雾 | D. | 铁丝在氧气中剧烈燃烧,火星四溅 |
7.作为标准的碳原子质量为1.993×10-26kg,甲原子质量是这种碳原子质量的2倍,下列有关说法正确的是( )
| A. | 甲的相对原子质量为2 | |
| B. | 甲的原子质量为3.32×10-27kg | |
| C. | 甲的相对原子质量为24 | |
| D. | 甲的相对原子质量为3.986×10-26kg |
4.下列实验操作中,正确的是( )
| A. |  氧气验满 | B. |  过滤 | C. |  倾倒液体 | D. |  稀释浓硫酸 |
11.以下存放和取用药品的方法不合理的是( )
| A. | 食盐存放于广口瓶中 | B. | 蒸馏水存放于细口瓶中 | ||
| C. | 用镊子夹取石灰石颗粒 | D. | 用镊子取用碳酸钠粉末 |
5.前者是纯净物,后者是混合物的一组是( )
| A. | 五氧化二磷、氮气 | B. | 糖水、白酒 | C. | 干冰、矿泉水 | D. | 碘酒、液态氧 |
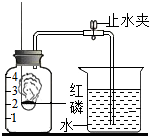 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下: