题目内容
6.在盛有一定质量的碳酸钙固体的锥形瓶中,滴加稀盐酸至没有气泡产生为止,刚好用去69.5mL(密度为1.05g/cm3)质量分数为10%的盐酸.求反应后所得溶液中溶质的质量分数.(最后结果精确到0.1%)分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据反应的化学方程式和提供的数据可以计算反应后所得溶液中溶质的质量分数.
解答 解:设碳酸钙质量为x,生成氯化钙质量为y,生成二氧化碳质量为z,
反应的氯化氢质量为:69.5mL×1.05g/cm3×10%=7.3g,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 111 44
x 7.3g y z
$\frac{100}{x}$=$\frac{73}{7.3g}$=$\frac{111}{y}$=$\frac{44}{z}$,
x=10g,y=11.1g,z=4.4g,
反应后溶液的质量为:10g+69.5mL×1.05g/cm3-4.4g=78.6g,
反应后所得溶液中溶质的质量分数为:$\frac{11.1g}{78.6g}$×100%=14.1%,
答:反应后所得溶液中溶质的质量分数为14.1%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18. 我校“非常化学”兴趣小组同学在实验室拍下一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
我校“非常化学”兴趣小组同学在实验室拍下一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是A.
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.
Ⅱ.Na2CO3和NaHCO3溶液都呈碱性.
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
【得出结论】小华根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是NaHCO3.
【作出猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl.
【设计并实验】
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,这瓶试剂不可能是③.
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验:
(3)请你选择与小强不同类别的试剂,来鉴别NaOH溶液和Na2CO3溶液,你选择Ca(OH)2溶液.
 我校“非常化学”兴趣小组同学在实验室拍下一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
我校“非常化学”兴趣小组同学在实验室拍下一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是A.
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.
Ⅱ.Na2CO3和NaHCO3溶液都呈碱性.
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
【作出猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl.
【设计并实验】
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,这瓶试剂不可能是③.
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取少量该溶液于一洁净试管中滴加氯化钡溶液 | 产生白色沉淀 | 猜想②正确 相关的化学方程式BaCl2+Na2CO3═BaCO3↓+2NaCl. |
17.某校化学兴趣小组同学测定大理石样品中碳酸钙的质量分数.准确称量20g大理石样品放入烧杯中,向烧杯中加入100mL过量的稀盐酸(杂质不反应),立即将烧杯放到电子秤上称量,记录数据如表.
(1)从表中可知,化学反应速度的变化趋势是越来越慢,原因是稀盐酸的质量分数越来越小.
(2)计算大理石样品中碳酸钙的质量分数(写出计算过程).
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 质量/g | 170.00 | 166.00 | 164.00 | 163.00 | 162.40 | 162.08 | 162.08 |
(2)计算大理石样品中碳酸钙的质量分数(写出计算过程).
1.镍氢充电电池有着广泛应用,镍及其化合物能发生下列反应:①Ni+2HCl=NiCl2+H2↑ ②NiO+2HCl=NiCl2+H2O ③NiO2+4HCl=NiCl2+Cl2↑+2H2O. Ni(OH)2不溶于水.对上述反应的分析判断错误的是( )
| A. | 镍能与氯化铜溶液发生置换反应 | |
| B. | 反应①是置换反应 | |
| C. | NiCl2能与NaOH溶液发生反应生成物中有沉淀 | |
| D. | 反应②中Ni的化合价发生了变化 |
18.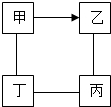 如图中“-”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以直接转化为乙.下面四组选项中,符合如图要求的是( )
如图中“-”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以直接转化为乙.下面四组选项中,符合如图要求的是( )
 如图中“-”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以直接转化为乙.下面四组选项中,符合如图要求的是( )
如图中“-”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以直接转化为乙.下面四组选项中,符合如图要求的是( ) | 甲 | 乙 | 丙 | 丁 | |
| A | H2SO4 | NaOH | NaCl | Na2CO3 |
| B | CO | CO2 | H2SO4 | CuO |
| C | Fe | Fe2(SO4)3 | Mg | HCl |
| D | O2 | CO | CuO | C |
| A. | A | B. | B | C. | C | D. | D |
16.把金属镍(Ni)、锰(Mn)分别放人下列化合物溶液中,反应的结果如表:
则它们的金属活动性由强到弱的顺序为( )
| 溶液 金属 | MgCl2溶液 | Ni的化合物溶液 | CuS04溶液 |
| Ni | 无金属析出 | - | 有金属析出 |
| Mn | 无金属析出 | 有金属析出 | 有金属析出 |
| A. | Mg Ni Mn Cu | B. | Cu Ni Mn Mg | C. | Cu Mn Ni Mg | D. | Mg Mn Ni Cu |
 多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界.
多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界.