题目内容
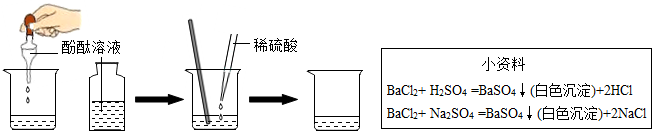
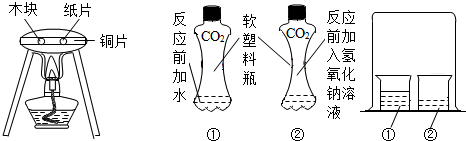
 用紫色石蕊试液将滤纸染成紫色,经烘干后做成两朵干燥紫色小花.如图,先取一朵直接放入盛有二氧化碳的集气瓶中,再取另一朵喷上水后再放入盛有二氧化碳的集气瓶中.
用紫色石蕊试液将滤纸染成紫色,经烘干后做成两朵干燥紫色小花.如图,先取一朵直接放入盛有二氧化碳的集气瓶中,再取另一朵喷上水后再放入盛有二氧化碳的集气瓶中.(1)观察到集气瓶内的现象分别是:第一朵小花
(2)取出第二朵小花加热,观察到的现象是
(3)简述你观察到的实验证据,说明使紫色石蕊变红的物质究竟是什么?并写出相关反应的化学方程式
考点:二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:碳单质与含碳化合物的性质与用途
分析:(1)根据二氧化碳不能使紫色石蕊变红色,二氧化碳和水反应生成的碳酸能使紫色石蕊变红色解答;
(2)根据碳酸受热分解为水和二氧化碳解答;
(3)根据二氧化碳和水反应生成碳酸解答.
(2)根据碳酸受热分解为水和二氧化碳解答;
(3)根据二氧化碳和水反应生成碳酸解答.
解答:解:(1)二氧化碳不能使紫色石蕊变红色,二氧化碳和水反应生成的碳酸能使紫色石蕊变红色;
(2)碳酸受热分解为水和二氧化碳,红色变为紫色;
(3)二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊变红色;
故答案:(1)不变色;变红色;(2)红色变为紫色;H2CO3═CO2↑+H2O;(3)CO2+H2O═H2CO3.
(2)碳酸受热分解为水和二氧化碳,红色变为紫色;
(3)二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊变红色;
故答案:(1)不变色;变红色;(2)红色变为紫色;H2CO3═CO2↑+H2O;(3)CO2+H2O═H2CO3.
点评:本题对实验室气体的制取装置进行了探究,在对二氧化碳性质的探究上,针对教材实验不足的基础上,采取了类似“控制变量”的操作方法,对可能使石蕊变红的物质--水、二氧化碳、碳酸逐一探究.

练习册系列答案
相关题目
日常生活中常见的铁桶,可以用该桶盛放的是( )
| A、盐酸 | B、稀硫酸 |
| C、水 | D、硫酸铜溶液 |
当发生紧急情况时,下列做法合理的是( )
| A、厨房内天然气泄漏,立即关闭阀门、开窗通风 |
| B、酒精灯被碰倒起火,立即撤离实验室 |
| C、炒菜时油锅着火,立即浇水灭火 |
| D、浓硫酸沾到手上,马上配制3%-5%的碳酸氢钠溶液来涂抹 |
“酒驾”是当前热门话题之一.酒精检测仪用于检查司机呼出的气体中的酒精含量是否超标,其原理可表示为C2H5OH+4CrO3+6H2SO4=2X+2CO2+9H2O,红色的三氧化铬变为绿色的硫酸铬(用X表示),则硫酸铬的化学式为( )
| A、H2Cr2O7 |
| B、Cr2(SO4)3 |
| C、CrSO4 |
| D、Cr2O3 |