题目内容
如图1硝酸铵(NH4NO3)无毒,可作农肥.硝酸铵适用的土壤和作物范围广,但最适于旱地和旱作物对烟、棉、菜等经济作物尤其适用.在温度达到230℃时硝酸铵会发生分解反应,生成相对分子质量最小的氧化物和氧气、以及一种单质.

(1)硝酸铵在230℃时发生分解反应的表达式:
(2)硝酸铵的相对分子质量
(3)硝酸铵中氮元素:氢元素:氧元素的质量比
(4)建立一个适当的模型来反映和代替客观现象,可以更简单明了地表示事物.
甲图是人体中元素质量分数模型,则A代表的一种元素是
小明模仿图1甲构建了NH4NO3中各元素质量分数的模型(如图1乙),则图1乙中表示氮元素的是
(5)农户老张购买了一袋200kg的硝酸铵,这些化肥最多能为庄稼提供多少千克氮元素?

(1)硝酸铵在230℃时发生分解反应的表达式:
2NH4NO3
2N2↑+O2↑+4H2O
| ||
2NH4NO3
2N2↑+O2↑+4H2O
.
| ||
(2)硝酸铵的相对分子质量
80
80
.(3)硝酸铵中氮元素:氢元素:氧元素的质量比
7:1:12
7:1:12
.(4)建立一个适当的模型来反映和代替客观现象,可以更简单明了地表示事物.
甲图是人体中元素质量分数模型,则A代表的一种元素是
O
O
.(填元素符号)小明模仿图1甲构建了NH4NO3中各元素质量分数的模型(如图1乙),则图1乙中表示氮元素的是
B
B
(选填A、B、C)(5)农户老张购买了一袋200kg的硝酸铵,这些化肥最多能为庄稼提供多少千克氮元素?
分析:(1)根据化学反应中元素种类不变,可以确定生成物种类再书写方程式;(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答;(3)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;(4))运用人体中各元素的含量解答;运用根据化学式计算该化合物中各元素的质量比解答;(5)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:(1)相对原子质量最小的元素是氢,所以相对分子质量最小的氧化物是H2O,根据质量守恒定律可以知道:化学反应中元素的种类不变,反应物中含有氮元素,因此生成物中应该含有氮元素,所以含氮元素的单质是氮气,因此硝酸铵在温度达到230℃时硝酸铵会发生分解反应,生成水、氮气和氧气,该反应的化学方程式为:2NH4NO3
2N2↑+O2↑+4H2O;
(2)硝酸铵的相对分子质量是14×2+1×4+16×3=80;
(3)硝酸铵中的N、H、O质量比是(14×2):(1×4):(16×3)=7:1:12;
(4)人体中含量最多的物质是水,水中氢氧元素的质量比是1:8,故人体中含量最多的元素是氧元素;
NH4NO3中H:N:O=1×4:14×2:16×3=4:28:48=1:7:12,所以在硝酸铵中氧元素含量最多,其次是氮元素,最少的是氢元素,故答案:B;
(5)200kg硝酸铵中含有氮元素的质量为200kg×
×100%=70kg
故答案为:(1)2NH4NO3
2N2↑+O2↑+4H2O;(2)80;(3)7:1:12;(4)O;B;(5)70kg.
| ||
(2)硝酸铵的相对分子质量是14×2+1×4+16×3=80;
(3)硝酸铵中的N、H、O质量比是(14×2):(1×4):(16×3)=7:1:12;
(4)人体中含量最多的物质是水,水中氢氧元素的质量比是1:8,故人体中含量最多的元素是氧元素;
NH4NO3中H:N:O=1×4:14×2:16×3=4:28:48=1:7:12,所以在硝酸铵中氧元素含量最多,其次是氮元素,最少的是氢元素,故答案:B;
(5)200kg硝酸铵中含有氮元素的质量为200kg×
| 28 |
| 80 |
故答案为:(1)2NH4NO3
| ||
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力,做题时找准思路和知识点,题目的难点就会不攻自破.

练习册系列答案
相关题目
Ⅰ.成年人每分钟大约需要吸入8L氧气.问成年人每分钟大致需要空气 升;在标准状况下,8L氧气的质量是 克;所需空气的质量为 克;(空气中氧气体积分数按20%计算,氧气的密度=1.429g?L-1,空气的密度=1.293g?L-1).
Ⅱ.小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强想通过计算氮的质量分数判断该广告是否
为虚假广告.
Ⅱ.小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强想通过计算氮的质量分数判断该广告是否
为虚假广告.
| 国内首创 优质硝酸铵 NH4 NO3 含氮量全球最高(38%)(1)请你写出小强的计算过程和判断依据.计算过程: 结论:该广告 (2)小强认为此广告会坑害农民,向有关部门反映,技术监督局对该产品取样分析,发现氮元素质量分数仅为28%,则该产品中硝酸铵的质量分数为 |
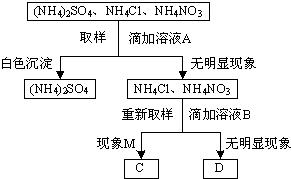 19、为鉴别(NH4)2SO4、NH4Cl、NH4NO3这三种固体样品,某同学分别取样配制成溶液并设计了如图所示的实验方案.
19、为鉴别(NH4)2SO4、NH4Cl、NH4NO3这三种固体样品,某同学分别取样配制成溶液并设计了如图所示的实验方案. (2013?沈阳)如图是某同学鉴别碳酸氢铵、硫酸铵、硝酸铵三种化肥的过程(反应条件未标出),请回答下列问题:
(2013?沈阳)如图是某同学鉴别碳酸氢铵、硫酸铵、硝酸铵三种化肥的过程(反应条件未标出),请回答下列问题: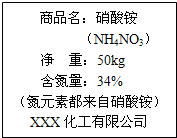 如图是某硝酸铵产品包装袋上的标签说明.仔细分析标签说明,然后回答下列有关问题.(解题时,均要列出计算过程)
如图是某硝酸铵产品包装袋上的标签说明.仔细分析标签说明,然后回答下列有关问题.(解题时,均要列出计算过程)