题目内容
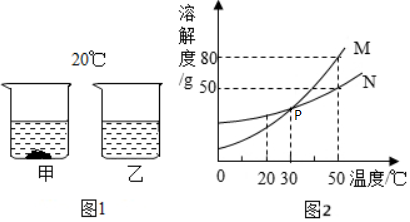
20.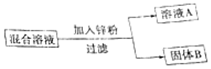 某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体B的成分迸行了分析和实验探究
某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体B的成分迸行了分析和实验探究(1)溶液A中一定含有的溶质是什么?
(2)若向固体B中加人稀盐酸,有气泡冒出,写出固体B的成分,写出其中发生的一个化学方程式.
分析 根据金属活动性顺序及其运用分析.排在氢之前的金属可与稀盐酸或稀硫酸反应产生氢气,排在前面的金属(除钾、钙、钠外)可将排在后面的金属从其盐溶液中置换出来.
解答 解:(1)根据金属活动性顺序:Zn>(H)>Cu>Ag可知,向AgNO3和Cu(NO3)2混合溶液中加入锌粉,Zn应先与AgNO3反应后与Cu(NO3)2反应,由于锌粉量的不同,溶液A中的溶质不同,溶液中的溶质可能是:只有Zn(NO3)2或Zn (NO3)2、Cu(NO3)2 或Zn (NO3)2、AgNO3、Cu(NO3)2,但是溶液中一定有Zn(NO3)2,
(2)因向固体B加盐酸有气体生成,所以固体B中一定有锌,故固体B为Ag、Cu和Zn,锌与盐酸反应生成氯化锌和氢气,化学方程式为:Zn+2HCl=ZnCl2+H2↑;
故答案为:(1)Zn(NO3)2;
(2)Ag、Cu和Zn;Zn+2HCl=ZnCl2+H2↑.
点评 本题难度不是很大,主要考查了对金属活动性顺序的应用和理解,培养学生的应用能力和解决问题的能力.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
10.石墨烯是由碳原子构成的纳米材料,有良好的强度、柔韧、导电、导热和光学特性.下列关于石墨烯的说法错误的是( )
| A. | 石墨烯可作电极材料 | B. | 石墨烯是一种金属 | ||
| C. | 石墨烯可用于制作包装袋 | D. | 石墨烯完全燃烧生成二氧化碳 |
11.在拓展性课程活动中,小明利用以下常见物品验证酸的一些性质:
白醋(含3%的醋酸)、食品干燥剂(主要成分是CaO)、鸡蛋壳、牵牛花汁液、铁钉、苏打(碳酸钠).
【查阅资料】牵牛花汁液在酸性溶液中显红色,在中性溶液中显紫色,在碱性溶液中显蓝色.
【实验过程】
(1)在鸡蛋壳上滴加白醋,产生无色、无味的气体,该气体能使澄清石灰水变浑浊.则鸡蛋壳中一定含有C${{O}_{3}}^{2-}$.(用离子符号表示)
(2)小明知道酸能够与铁发生反应产生氢气,但当他将足量的白醋加入放有铁钉的容器中,没有看到明显的气泡产生.小明很疑惑,于是提出猜想:气泡不明显可能与酸的浓度有关.要验证与酸的浓度有关,应选择下例试剂中的B.(选填编号)
A.3%的盐酸 B.5%的醋酸 C.5%的盐酸
(3)小明利用已有物品还想验证酸与碱的反应,请你帮助完成下列实验设计.
【评价反思】科掌来源于生活,生活中的许多事物能更好地帮助我们学习和理解科学.
白醋(含3%的醋酸)、食品干燥剂(主要成分是CaO)、鸡蛋壳、牵牛花汁液、铁钉、苏打(碳酸钠).
【查阅资料】牵牛花汁液在酸性溶液中显红色,在中性溶液中显紫色,在碱性溶液中显蓝色.
【实验过程】
(1)在鸡蛋壳上滴加白醋,产生无色、无味的气体,该气体能使澄清石灰水变浑浊.则鸡蛋壳中一定含有C${{O}_{3}}^{2-}$.(用离子符号表示)
(2)小明知道酸能够与铁发生反应产生氢气,但当他将足量的白醋加入放有铁钉的容器中,没有看到明显的气泡产生.小明很疑惑,于是提出猜想:气泡不明显可能与酸的浓度有关.要验证与酸的浓度有关,应选择下例试剂中的B.(选填编号)
A.3%的盐酸 B.5%的醋酸 C.5%的盐酸
(3)小明利用已有物品还想验证酸与碱的反应,请你帮助完成下列实验设计.
| 步骤 | 操作 | 现象 |
| 1 | 将食品干燥剂加入适量清水中,搅拌后静置 | 放出大量的热 |
| 2 | 取步骤1中的上层清液,先加入牵牛花汁液,滴加白醋 | 溶液由无色变为蓝色,再变为紫色,最后变为红色 |
8.下列是化学实验基本操作的图示.其中正确的是( )
| A. | 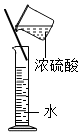 浓硫酸的稀释 | B. | 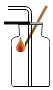 收集CO2时验满 | ||
| C. | 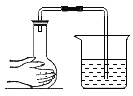 检查装置的气密性 | D. | 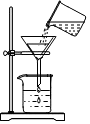 过滤操作 |
11.W、X、Y、Z四种物质在一定条件下充分反应后,测得反应前后各物质的质量如下:
下列说法错误的是( )
| 物质 | W | X | Y | Z |
| 反应前质量/g | 1.8 | 22 | 34 | 0 |
| 反应后质量/g | 1.8 | 40 | 未知 | 16 |
| A. | 反应生成40g的X | B. | “未知”的值是0 | ||
| C. | W可能是反应的催化剂 | D. | Y一定是化合物 |