题目内容
14.构建知识网络可帮助我们理解知识间的联系.图1是盐酸与不同类别物质之间反应的知识网络.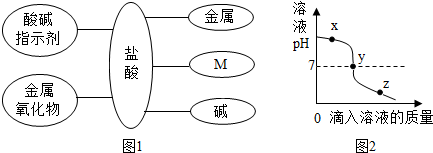
(1)图中M应为盐类物质(填物质类属).
(2)写出一种能与盐酸反应的金属锌.
(3)用盐酸除铁锈(主要成分Fe2O3)的化学方程式是Fe2O3+6HCl═2FeCl3+3H2O.
(4)微观角度看,HCl与碱(如NaOH)反应实质是H+与OH-等微粒结合为水.
(5)现有盐酸、滴有酚酞的氢氧化钠溶液两种溶液,取其中一种溶液置于烧杯中,用胶头滴管取另一种溶液并逐滴加入到烧杯中直至过量.图2表示此过程中胶头滴管滴入溶液的质量与烧杯中溶液pH变化的变化关系,有关说法不正确的是B.
A.放置于烧杯中的溶液为含酚酞的氢氧化钠溶液
B.x点时,烧杯中的溶液只含有一种溶质
C.y点表示盐酸和氢氧化钠恰好完全反应
D.y点和z点时,溶液均呈现无色.
分析 把盐酸的性质用网络框架的形式表示出来,可以更直观的让学生了解和记忆.根据盐酸的化学性质:①跟指示剂反应 ②跟活泼金属起置换反应 ③跟碱性氧化物反应 ④跟某些盐反应 ⑤跟碱起中和反应.氢氧化钠和盐酸反应生成氯化钠和水,此反应属于复分解反应,酸碱中和的实质是酸中的氢离子和碱中的氢氧根离子结合生成了水分子;
根据图象2中的曲线可以知道起始溶液的pH值大于7,而反应后溶液的pH值小于7,可以判断是向氢氧化钠溶液中滴加稀盐酸
解答 解:(1)盐酸可与五类物质发生化学反应,图中M应为其中的盐类物质;
故答案为:盐;
(2)在金属活动性顺序中排在氢前面的金属都能和盐酸反应,常用的有铝镁锌铁;
故答案为:锌;
(3)铁锈属于金属氧化物,与盐酸反应生成盐和水,反应中元素的化合价不变;
故答案为:Fe2O3+6HCl═2FeCl3+3H2O;
(4)氢氧化钠溶液和盐酸反应生成氯化钠和水,为中和反应,中和反应的实质是酸中的氢离子和碱中的氢氧根离子结合生成了水分子;
故答案为:H+、OH-;
(5)根据图象中的曲线可以知道起始溶液的pH值大于7,而反应后溶液的pH值小于7,可以判断是向氢氧化钠溶液中滴加稀盐酸,故A正确;
x点时,氢氧化钠有剩余,故溶液中的溶质有氢氧化钠和氯化钠,故B错误;
y点pH=7,表示盐酸和氢氧化钠恰好完全反应,故C正确;
y点和z点时,溶液分别为中性和酸性,均呈现无色,故D正确;
故选B.
点评 盐酸是酸的代表物质,要熟记酸的通性,要求同学们能写出每一项性质的化学方程式.

练习册系列答案
相关题目
5.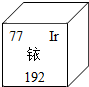 今年央视3.15晚会揭开周大生等品牌黄金制品掺杂铱牟取暴利的内幕.铱元素在周期表中的信息如图所示.下列说法不正确的是( )
今年央视3.15晚会揭开周大生等品牌黄金制品掺杂铱牟取暴利的内幕.铱元素在周期表中的信息如图所示.下列说法不正确的是( )
 今年央视3.15晚会揭开周大生等品牌黄金制品掺杂铱牟取暴利的内幕.铱元素在周期表中的信息如图所示.下列说法不正确的是( )
今年央视3.15晚会揭开周大生等品牌黄金制品掺杂铱牟取暴利的内幕.铱元素在周期表中的信息如图所示.下列说法不正确的是( )| A. | 铱属于金属元素 | B. | 铱的原子序数是77 | ||
| C. | 铱原子的核外电子数为77 | D. | 铱原子相对原子质量是192g |
19.在一密闭容器内有氧气、二氧化碳、水蒸气和一种未知物W,在一定条件下充分反应,测得反应前后各物质的质量如下表所示,则下列说法中错误的是( )
| 物 质 | 氧 气 | 二氧化碳 | 水蒸气 | W |
| 反应前质量/g | 50 | 1 | 1 | 23 |
| 反应后质量/g | 2 | 45 | 28 | x |
| A. | x的值应为0 | B. | 二氧化碳是生成物 | ||
| C. | 23gW中氢元素质量为6g | D. | W由C、H、O三种元素组成 |
6.La(镧)是一种活动性比锌强的金属元素,其氧化物为La2O3,对应的碱La(OH)3难溶于水,而LaCl3、La(NO3)3都易溶于水.下列各组物质中,不能直接反应生成LaCl3的是( )
| A. | La+HCl | B. | La2O3+HCl | C. | NaCl+La(NO3)3 | D. | La(OH)3+HCl |