题目内容
3.焦亚硫酸钠有毒,不能直接用于食品加工,市场上有不法商贩将其溶液浸泡生姜,使生姜发黄发亮,食用此种生姜可能使人中毒,已知焦亚硫酸钠的化学式为Na2S2Ox,相对分子质量是190,请计算:(1)x=5;
(2)焦亚硫酸钠中硫元素与氧元素的质量比是4:5;
(3)焦亚硫酸钠中钠元素的质量分数是24.2%(精确到0.1%物质)
分析 (1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
解答 解:(1)焦亚硫酸钠的对分子质量为23×2+32×1+16×x=190,x=5.
(2)焦亚硫酸钠中硫元素与氧元素的质量比是(32×2):(16×5)=4:5.
(3)焦亚硫酸钠中钠元素的质量分数是$\frac{23×2}{190}$×100%≈24.2%.
故答案为:(1)5;(2)4:5;(3)24.2%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
14.炭雕(如图所示)即是一种工艺品,又是一种实用的室内空气净化器.它具有空气净化功能源于( )


| A. | 活性炭的吸附性 | B. | 碳的稳定性 | C. | 碳的导电性 | D. | 碳的氧化性 |
11.下列实验操作中,正确的是( )
| A. |  读取液体体积 | B. |  闻药品味道 | C. |  点燃酒精灯 | D. |  滴加液体 |
12.在哥本哈根召开了世界气候大会,各国共同协商对策,以减少温室气体排放量.下列气体中大家关注的温室气体是( )
| A. | 氮气 | B. | 氧气 | C. | 氢气 | D. | 二氧化碳 |
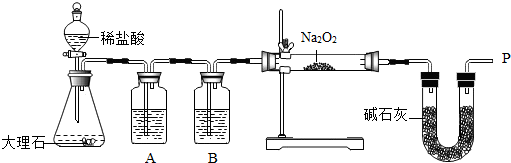
18.某化学兴趣小组利用如图所示装置进行“过氧化钠(Na2O2)与CO2反应”等实验探究活动.装置气密性良好,所用试剂均足量.装置内的空气对实验的影响可以忽略.实验所用过氧化钠药品中所含杂质不参加化学反应.已知:(1).碱石灰是由固体NaOH和CaO组成的混合物.
(2).NaHCO3不与CO2反应.饱和NaHCO3溶液可吸收HCl气体.
(3).过氧化钠是一种淡黄色粉末状固体,Na2O2能与CO2反应:2Na2O2+2CO2═2Na2CO3+O2,也能与H2O反应:2Na2O2+2H2O═4NaOH+O2↑.
主要探究过程记录如下:
有关数据记录如下:玻璃管中过氧化钠药品的质量为m,操作Ⅱ再次测得玻璃管内固体质量n.
请回答下列问题:
(1)锥形瓶中发生反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)若A瓶所装试剂是饱和NaHCO3溶液,则B瓶所装试剂是浓硫酸.
(3)操作Ⅰ空白处记录的实验现象是带火星的木条复燃.
(4)操作Ⅱ“烧杯中无明显现象”说明过氧化钠完全反应.
(5)药品中过氧化钠的质量分数用m和n的代数式表示为$\frac{15600(n-m)}{56m}$%.
(2).NaHCO3不与CO2反应.饱和NaHCO3溶液可吸收HCl气体.
(3).过氧化钠是一种淡黄色粉末状固体,Na2O2能与CO2反应:2Na2O2+2CO2═2Na2CO3+O2,也能与H2O反应:2Na2O2+2H2O═4NaOH+O2↑.

主要探究过程记录如下:
| 实验操作 | 实验现象 |
| Ⅰ.打开分液漏斗旋塞,向锥形瓶中注入足量稀盐酸后关闭;一段时间后在导管口P处用带火星的木条检验导出的气体 | 锥形瓶内产生大量气泡 |
| Ⅱ.观察到玻璃管内固体变为白色后,再次测定玻璃管内固体质量;测定固体质量完毕后将固体溶于盛有适量水的烧杯中 | 烧杯中无明显现象 |
请回答下列问题:
(1)锥形瓶中发生反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)若A瓶所装试剂是饱和NaHCO3溶液,则B瓶所装试剂是浓硫酸.
(3)操作Ⅰ空白处记录的实验现象是带火星的木条复燃.
(4)操作Ⅱ“烧杯中无明显现象”说明过氧化钠完全反应.
(5)药品中过氧化钠的质量分数用m和n的代数式表示为$\frac{15600(n-m)}{56m}$%.
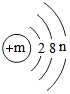 (其中n≠0),若m-n=10,则该粒子对应的常见金属元素有
(其中n≠0),若m-n=10,则该粒子对应的常见金属元素有