题目内容
16.某学习小组为探究某高锰酸钾样品中高锰酸钾的质量分数,加热 10g高锰酸钾样品,至不再反应为止,称得剩余固体的质量为9.36g.求:(1)生成O2的质量是0.64g.
(2)此样品中高锰酸钾的质量分数为(写出计算过程)
分析 (1)根据质量守恒定律计算生成氧气的质量;
(2)根据化学方程式和氧气的质量,计算参加反应的高锰酸钾的质量.
解答 解:(1)生成氧气的质量为:10g-9.36g=0.64g;
(2)设样品中高锰酸钾的质量为x
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 0.64g
$\frac{316}{x}$=$\frac{32}{0.64g}$
x=6.32g
所以样品中高锰酸钾的质量分数为:$\frac{6.32g}{10g}$×100%=63.2%.
故答案为:此样品中高锰酸钾的质量分数为63.2%.
点评 解答本题的关键是根据质量守恒定律可知试管内质量的减少量就是生成氧气的质量,根据氧气的质量再计算高锰酸钾的质量即可.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
9.下列变化过程中,一定发生化学变化的是( )
| A. | 西瓜榨汁 | B. | 工业制氧气 | C. | 玉米酿酒 | D. | 爆炸 |
11.在点燃条件下,A和B反应生成C和D.反应前后分子种类变化的微观示意图如图:以下说法不正确的是( )
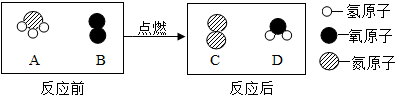

| A. | 这个化学反应共涉及到2种化合物 | |
| B. | 1个A分子中共含有有4个原子 | |
| C. | 在该反应中,生成C和D的质量比为14:27 | |
| D. | 在该反应中,生成C和D的质量比为14:9 |
8.小明在做过滤操作时,在老师给他的仪器中,他认为还缺少一种,其中老师给的仪器主要有:漏斗、烧杯、滤纸、铁架台(带铁圈),那么他认为缺少的仪器是( )
| A. | 小烧杯 | B. | 长颈漏斗 | C. | 药匙 | D. | 玻璃棒 |
下列物质性质与用途的对应关系错误的是( )
选项 | 性质 | 用途 |
A | 氧气具有助燃性 | 用于火箭发射 |
B | 浓硫酸具有腐蚀性 | 干燥氢气 |
C | 稀盐酸能与某些金属氧化物反应 | 除铁锈 |
D | 氢氧化钠能与某些非金属氧化物反应 | 吸收二氧化硫 |
A. A B. B C. C D. D
 通过实验及分析,确定该粉末为氧化铜和碳粉混合物,为了进一步探究它们的性质,探究小组又利用这种混合物补充做了如图所示实验:
通过实验及分析,确定该粉末为氧化铜和碳粉混合物,为了进一步探究它们的性质,探究小组又利用这种混合物补充做了如图所示实验: A~D是初中化学所学的常见物质,其转化关系如图所示(部分反应物和生成物、反应条件已略去),A、C常温下为无色气体且组成元素相同,B、D均为黑色粉末,且D是世界上年产量最大的金属.请回答下列问题:
A~D是初中化学所学的常见物质,其转化关系如图所示(部分反应物和生成物、反应条件已略去),A、C常温下为无色气体且组成元素相同,B、D均为黑色粉末,且D是世界上年产量最大的金属.请回答下列问题: