题目内容
8.在 440℃和高压条件下,金属钠与二氧化碳反应能生成金刚石(C)和碳酸钠,该反应的化学方程式为( )| A. | 4Na+3CO2↑═C+2Na2CO3 | B. | Na+CO2$\frac{\underline{\;440℃\;}}{高温}$C+Na2CO3 | ||
| C. | 2Na+3CO2$\frac{\underline{\;440℃\;}}{高压}$C+2NaCO3 | D. | 4Na+3CO2$\frac{\underline{\;440℃\;}}{高压}$C+2Na2CO3 |
分析 根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
解答 解:在440℃和高压条件下,金属钠与二氧化碳反应能生成金刚石(C)和碳酸钠,该反应的化学方程式为4Na+3CO2$\frac{\underline{\;440℃\;}}{高压}$C+2Na2CO3.
故选:D.
点评 本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断;化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.厨房炒菜,油锅不慎着火,下列灭火措施最适宜的是( )
| A. | 加水 | B. | 倒去油 | C. | 盖上锅盖 | D. | 撒上沙子 |
16.下列有关元素和原子的叙述正确的是( )
| A. | 元素是宏观概念,只论种类不讲个数,原子是微观概念,既论种类又讲个数 | |
| B. | 在化学反应中,元素可分而原子不可分 | |
| C. | 水是由氢元素和氧元素两个元素组成的 | |
| D. | 我们现在发现的元素种类大概有3000多万种 |
3.下列粒子结构示意图中,表示阳离子的是( )
| A. | 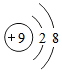 | B. | 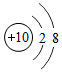 | C. | 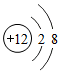 | D. | 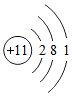 |
13.有X、Y、Z三种元素,它们的化合价分别是+1、+5、-2,由这三种元素组成的化合物的化学式可能是( )
| A. | X3YZ3 | B. | X2YZ3 | C. | X4YZ3 | D. | X3YZ4 |
20.下列关于化学反应“X2+3Y2═2Z”的叙述正确的是( )
| A. | Z的化学式为X2Y3 | |
| B. | mg X2 和ng Y2 恰好完全反应,则一定生成(m+n)g Z | |
| C. | 若有ag X2 完全反应,生成bg Z,则同时消耗 (2b-a) g Y2 | |
| D. | 若X2 和Y2 的相对分子质量分别为M和N,则Z的相对分子质量为(M+N) |
17.小明对铁的锈蚀进行如下探究.室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图.观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL).当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零).记录起始和最终量筒的读数以及所需时间如表.
(1)实验①和②说明NaCl可以加快 (填“加快”或“减慢”)铁锈蚀的速率.
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是放热 (填“放热”或“吸热”)过程.
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是Fe2O3•xH2O[Fe2O3或Fe(OH)3];.
(4)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成.
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是20.5%(保留3位有效数字).
(6)现仅提供:置筒、大烧杯、玻璃棒、水、滤纸包(内含1g铁粉、O.2g碳、10滴水和少量NaCl),请你帮助小明再设计一个测量空气中氧气体积含量的实验方案,在图中画出实验装置示意图即可(注明滤纸包的位置).

| 序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
| ① | 1 g铁粉、0.2 g碳和10滴水 | 100 | 70 | 约120 |
| ② | l g铁粉、0.2 g碳、10滴水和少量NaCl | 100 | 70 | 约70 |
| ③ | | 0 | 0 | 0 |
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是放热 (填“放热”或“吸热”)过程.
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是Fe2O3•xH2O[Fe2O3或Fe(OH)3];.
(4)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成.
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是20.5%(保留3位有效数字).
(6)现仅提供:置筒、大烧杯、玻璃棒、水、滤纸包(内含1g铁粉、O.2g碳、10滴水和少量NaCl),请你帮助小明再设计一个测量空气中氧气体积含量的实验方案,在图中画出实验装置示意图即可(注明滤纸包的位置).

18.某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成.分四次取样品与稀硫酸反应,其实验数据记录如表.
试计算:
(1)在四份样品所做的实验中,硫酸有剩余的是3、4;
(2)列式计算所用稀硫酸中溶质的质量分数
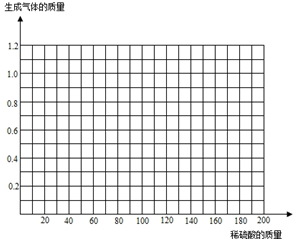
(3)请在图中画出在50.0g样品中加入稀硫酸的质量与产生气体质量变化关系的示意图.
(4)请计算恰好完全反应时溶液中溶质的质量分数.
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量 | 0.4 | 0.8 | 1.0 | 1.0 |
(1)在四份样品所做的实验中,硫酸有剩余的是3、4;
(2)列式计算所用稀硫酸中溶质的质量分数
(3)请在图中画出在50.0g样品中加入稀硫酸的质量与产生气体质量变化关系的示意图.

(4)请计算恰好完全反应时溶液中溶质的质量分数.