题目内容
人类的生产生活离不开金属,下列三种金属使用的先后顺序依次为:铜、铁、铝.
(1)金属被使用的先后顺序跟 (填序号)选项关系最大.
①地壳中金属元素的含量;②金属的导电性;③金属的活动性.
(2)为探究锰与铁的金属活动性,在相同温度下,取大小相同、表面光亮的两种金属薄片,分别投入等体积、等溶质的质量分数的足量稀盐酸中(反应中Mn显+2价),请回答:
除了比较与酸反应产生气体速率的快慢,请你再举出一种可比较这二种金属活动性强弱的方法(写出所需药品即可): .
(3)将一定量的铝加入到硫酸亚铁和硫酸铜的混合溶液中,充分反应后过滤,向滤渣中加入盐酸,有气泡产生.则滤渣中一定有的物质是 .(填化学式)
(1)金属被使用的先后顺序跟
①地壳中金属元素的含量;②金属的导电性;③金属的活动性.
(2)为探究锰与铁的金属活动性,在相同温度下,取大小相同、表面光亮的两种金属薄片,分别投入等体积、等溶质的质量分数的足量稀盐酸中(反应中Mn显+2价),请回答:
| 金 属 | 铁 | 锰 |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 |
| 结 论 | 活动性铁 | |
(3)将一定量的铝加入到硫酸亚铁和硫酸铜的混合溶液中,充分反应后过滤,向滤渣中加入盐酸,有气泡产生.则滤渣中一定有的物质是
考点:金属活动性顺序及其应用,金属的化学性质
专题:金属与金属材料
分析:(1)金属活动性较弱时,难形成化合物,常以单质形式存在,比较容易被利用;金属的活动性越强,就越难把它制成单质,使用的就晚.
(2)只有前面的金属可以把排在它后面的金属从盐溶液中置换出来,根据这一规律可以设计实验来验证金属的活动性顺序.
(3)根据金属活动性顺序表的应用分析回答.
(2)只有前面的金属可以把排在它后面的金属从盐溶液中置换出来,根据这一规律可以设计实验来验证金属的活动性顺序.
(3)根据金属活动性顺序表的应用分析回答.
解答:解:(1)在金属活动性顺序中,化学性质越活泼的金属越易和空气中的成分发生化学变化,因此主要以化合物的形式存在于自然界中,就越难以发现,所以,金属大规模被使用的先后顺序跟金属的活动性的关系最大.
(2)由于铁和稀盐酸反应时放出气泡的速率慢,说明铁的活动性比锰弱;验证金属的活动性顺序,除了使用金属和酸溶液反应外,也可以采用金属和盐溶液,例如,可以使用FeSO4、Mn(或Fe、Mn(NO3)2).
(3)根据金属活动顺序表可知,铝比铁活泼,铁比铜活泼.所以,加入一定量的铝,首先铝和硫酸铜溶液反应,置换出单质铜,如果铝足量可以继续与硫酸亚铁反应置换出铁.由题意可知,向滤出的固体中滴加盐酸,有气泡产生,说明固体中含有和盐酸反应的金属,由题可知,金属可能是铁或铁和铝.所以,则滤渣中一定有的物质是Fe、Cu.
故答为:(1)③;(2)<FeSO4、Mn(或Fe、Mn(NO3)2) (3)Fe、Cu
(2)由于铁和稀盐酸反应时放出气泡的速率慢,说明铁的活动性比锰弱;验证金属的活动性顺序,除了使用金属和酸溶液反应外,也可以采用金属和盐溶液,例如,可以使用FeSO4、Mn(或Fe、Mn(NO3)2).
(3)根据金属活动顺序表可知,铝比铁活泼,铁比铜活泼.所以,加入一定量的铝,首先铝和硫酸铜溶液反应,置换出单质铜,如果铝足量可以继续与硫酸亚铁反应置换出铁.由题意可知,向滤出的固体中滴加盐酸,有气泡产生,说明固体中含有和盐酸反应的金属,由题可知,金属可能是铁或铁和铝.所以,则滤渣中一定有的物质是Fe、Cu.
故答为:(1)③;(2)<FeSO4、Mn(或Fe、Mn(NO3)2) (3)Fe、Cu
点评:本题主要考查了学生对金属活动顺序表的运用,在解题时要注意对半定量(如一定量、过量、少量等)概念的理解和掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验的操作如图所示,其中正确的是( )
A、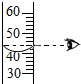 读取液体体积 |
B、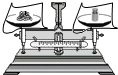 称量固体烧碱 |
C、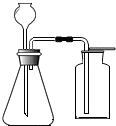 Zn和稀H2SO4制H2 |
D、 稀释浓硫酸 |
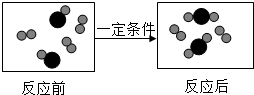
以下是一个化学反应的微观示意图,从示意图获取的信息错误的是( )
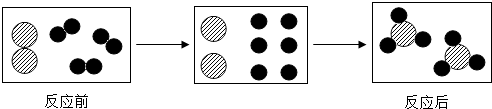

| A、反应前后分子种类发生改变 |
| B、反应前后原子的种类与数目不发生改变 |
| C、反应前两种分子的个数比是1:3 |
| D、该反应的基本类型是分解反应 |
下列物品的主要材料为有机合成材料的是( )
| A、纯棉帽子 | B、塑料水桶 |
| C、陶瓷餐具 | D、黄金饰品 |
物质的性质决定物质的用途,下列物质的用途与其化学性质有关的是( )
| A、氧气供给呼吸 |
| B、金刚石用作划玻璃 |
| C、铜作导线 |
| D、干冰用于人工降雨 |

 )与 B(
)与 B(  )反应生成C(
)反应生成C( ),下图是其反应前后分子及其数目变化的微观示意图(
),下图是其反应前后分子及其数目变化的微观示意图( 表示两种质子数不同的原子 ).
表示两种质子数不同的原子 ).