题目内容
下列对实验现象的分析合理的是
A. 向某无色溶液中滴入酚酞试液,呈红色,证明该溶液是碱溶液
B. 向某无色溶液中滴入硝酸银溶液,产生白色沉淀,证明该溶液是盐酸
C. 某白色固体与熟石灰混合后加热,产生可使湿润的红色石蕊试纸变蓝色的气体,证明该固体是铵盐
D. 向某固体中加入稀盐酸,产生无色气体。证明该固体中一定含有碳酸根离子
C 【解析】A、向某无色溶液中滴入酚酞试液,呈红色,证明该溶液是碱性溶液,不一定是碱,故A错误;B、向某无色溶液中滴入硝酸银溶液,产生白色沉淀,证明该溶液是盐酸或盐酸盐,故B错误;C、某白色固体与熟石灰混合后加热,产生可使湿润的红色石蕊试纸变蓝色的气体,应是氨气,氨气溶于水生成氨水,氨水呈碱性,氨气遇湿润的红色石蕊试纸变蓝色,证明该固体是铵盐,故C正确;D、向某固体中加入稀盐酸,产生无色气体...自动充气气球因使用方便,无需其它充气器材而逐渐得以推广。某化学兴趣小组对自动充气气球进行了如下探究。

(查阅资料)①自动充气气球的结构如图所示,气球的充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。
②氯化银是一种白色沉淀且不溶于稀硝酸。
(1)探究液体包的成分:
取液体包中的少量溶液分别放于两只于试管中,在其中一只试管中加入锌粒产生气泡,另一只试管中滴加硝酸银溶液,产生白色沉淀,继续滴加稀硝酸沉淀不溶,则小组同学证明液体包中装的是________,写出该液体与锌粒反应的化学方程式____________。
(2)探究白色粉末成分:
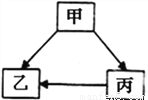
(猜想与假设)甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠。
(设计并进行实验)实验一:完成下表
操作步骤 | 现象 | 结论 |
甲同学的猜想不正确 |
实验二:按下图的实验装置,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的烧瓶中注入等体积、足量的稀盐酸,并测量生成二氧化碳的体积,记录如下表:

实验编号 | 锥形瓶内物质 | 最终得到CO2 体积/mL | |
名称 | 质量/g | ||
① | 碳酸氢钠 | 0.8 | V1 |
② | 碳酸钠 | 0.8 | V2 |
③ | 白色粉末 | a | V1 |
(3)实验装置中植物油的作用是___;表中a= ___;V1____V2(填“>”、“<”或“=”)。
(分析并得出结论)(4)分析上表中数据得出结论:白色粉末的成分是__________,依据是______。
盐酸 Zn+2HCl==ZnCl2+H2↑ 取少量白色粉末与试管中,加入足量的水溶解 固体完全溶解 使二氧化碳与水隔绝 a=8 V1V2 碳酸氢钠 等质量的白色粉末与碳酸氢钠生成的气体量相同 【解析】(1)探究液体包的成分:取液体包中的少量溶液分别放于两只于试管中,在其中一只试管中加入锌粒产生气泡,另一只试管中滴加硝酸银溶液,产生白色沉淀,继续滴加稀硝酸沉淀不溶,则证明液体包中装的是盐酸,盐...

 移走蒸发皿 B.
移走蒸发皿 B. 测溶液pH
测溶液pH  加热液体 D.
加热液体 D. 稀释浓硫酸
稀释浓硫酸