题目内容
新近,我国部分城市首次使用二甲醚作为公交车的燃料,有效解决了公交车冒黑烟的问题。二甲醚燃烧的化学方程式可表示为:CaHbOd(二甲醚)+ 3O2  2CO2 + 3H2O请通过计算回答:
2CO2 + 3H2O请通过计算回答:
(1)a = ;b = ;d = 。
(2)23g二甲醚充分燃烧需要多少克氧气?生成多少克二氧化碳?
(3)若用碳酸钠和稀硫酸反应,制取与(2)等质量的二氧化碳,需要质 量分数
量分数 为10%的稀硫酸(密度为1.1g/cm3)多少毫升?(计算结果保留小数点后一位)
为10%的稀硫酸(密度为1.1g/cm3)多少毫升?(计算结果保留小数点后一位)
 2CO2 + 3H2O请通过计算回答:
2CO2 + 3H2O请通过计算回答:(1)a = ;b = ;d = 。
(2)23g二甲醚充分燃烧需要多少克氧气?生成多少克二氧化碳?
(3)若用碳酸钠和稀硫酸反应,制取与(2)等质量的二氧化碳,需要质
 量分数
量分数 为10%的稀硫酸(密度为1.1g/cm3)多少毫升?(计算结果保留小数点后一位)
为10%的稀硫酸(密度为1.1g/cm3)多少毫升?(计算结果保留小数点后一位)(1)a= 2 ;b= 6 ;d= 1
(2)设23g二甲醚充分燃烧需要氧气质量为x,生成二氧化碳质量为y
C2H6O + 3O2 2CO2 + 3H2O
2CO2 + 3H2O
46 96 88
23g x y
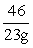 =
= 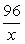
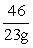 =
= 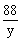
x = 48g
y = 44g
(3)设需要稀硫酸的质量为z
Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2↑
98 44
z 44g
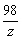 =
=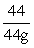
z = 98g
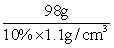 = 890.9 cm3 = 890.9 mL
= 890.9 cm3 = 890.9 mL
答:需要质量分数为10%的稀硫酸890.9mL
(2)设23g二甲醚充分燃烧需要氧气质量为x,生成二氧化碳质量为y
C2H6O + 3O2
 2CO2 + 3H2O
2CO2 + 3H2O 46 96 88
23g x y
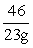 =
= 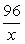
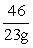 =
= 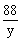
x = 48g
y = 44g
(3)设需要稀硫酸的质量为z
Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2↑
98 44
z 44g
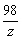 =
=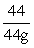
z = 98g
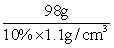 = 890.9 cm3 = 890.9 mL
= 890.9 cm3 = 890.9 mL 答:需要质量分数为10%的稀硫酸890.9mL

练习册系列答案
相关题目
 2CO2 + 3H2O
2CO2 + 3H2O 2CO2+3H2O
2CO2+3H2O 2CO2+3H2O
2CO2+3H2O