题目内容
20.下列物质暴露在空气中容易变质的是( )| A. | 浓硫酸 | B. | 硫酸铜粉末 | C. | 氧化铜粉末 | D. | 食盐晶体 |
分析 会变质即发生了化学变化,也就是与空气中的成分发生了化学反应.利用这一知识分析解决即可.
解答 解:A、浓硫酸不与空气中的成分反应,不会变质,错误;
B、硫酸铜粉末能与水反应生成五水硫酸铜,产生新的物质,容易变质,正确;
C、氧化铜粉末不与空气中的成分反应,不会变质,错误;
D、食盐晶体不与空气中的成分逆反应,不会变质,错误;
故选B.
点评 此题是对一些常见物质性质的考查,解决的关键是能对几种物质在空气中发生的化学变化有所了解,属基础性知识考查题.

练习册系列答案
相关题目
11.小丽同学在打扫实验室时发现窗台上有瓶敞口放置的NaOH溶液,小丽同学在征得老师的同意之后,对这瓶氢氧化钠溶液进行了探究实验.
【提出问题】这瓶NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】小丽猜想:NaOH溶液部分变质.你的猜想:全部变质(猜一种就可).
【实验探究】小丽设计如下实验,请根据表中内容填写小丽实验时的现象.
假设你的猜想正确,并按小丽的实验方案进行实验,则你观察到的实验现象有白色沉淀生成,溶液不变色.
【提出问题】这瓶NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】小丽猜想:NaOH溶液部分变质.你的猜想:全部变质(猜一种就可).
【实验探究】小丽设计如下实验,请根据表中内容填写小丽实验时的现象.
| 实验步骤 | 现 象 | 结 论 |
| 取少量NaOH溶液样品于试管中,先滴加足量的 氯化钙溶液,然后再滴加 酚酞试液. | 有白色沉淀生成 溶液变红 | NaOH溶液部分变质 |
8.某校化学兴趣小组在老师指导下探究孔雀石(一种铜矿石)的组成元素.他们取50克孔雀石粉末,在密闭容器中加热,观察到绿色的孔雀石逐渐变为黑色粉末,且有水和能使澄清石灰水变浑浊的气体产生,(已知:黑色粉末是一种金属氧化物,孔雀石中的杂质不反应,生成的二氧化碳全部被石灰水吸收).在二氧化碳被澄清石灰水吸收过程中他们测定相关数据如表:
请分析数据,回答下列问题:
(1)组成孔雀石的元素有铜元素、氢元素、氧元素和碳元素.
(2)表中“X”的值为15g.
(3)实验最终生成二氧化碳的质量是多少克(写出计算过程)?
| 测定次数 | 生成沉淀的质量(g) | 生成水的质量(g) |
| 1 | 5 | 0.9 |
| 2 | X | 2.7 |
| 3 | 20 | 3.6 |
| 4 | 20 | 3.6 |
(1)组成孔雀石的元素有铜元素、氢元素、氧元素和碳元素.
(2)表中“X”的值为15g.
(3)实验最终生成二氧化碳的质量是多少克(写出计算过程)?
15.地壳中含量最多的金属元素与含量最多的非金属元素组成的化合物为( )
| A. | SiO2 | B. | AlO | C. | Al2O3 | D. | Fe2O3 |
5.下列过程中发生了化学变化的是( )
| A. | 给轮胎打气 | B. | 粮食酿成酒 | C. | 铁铸造成锅 | D. | 海水晒盐 |
2.MCO3广泛应用于建筑工业.它能受热分解,也能与稀酸反应.为了确定MCO3中金属M的相对原子质量,某学习小组讨论了下列两种方案.
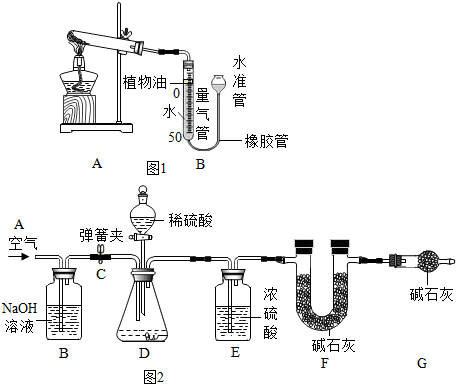
方案一:该小组中小梅设计如图1实验装置及步骤(友情提醒:MCO3═MO+CO2↑)
操作步骤:
①连接装置并检查装置的气密性;
②准确称量质量为10g 的MCO3;
③装好药品并调节量气装置两边液面相平,读数;
④加热至样品质量不再减少;
⑤冷却到室温;
⑥再次调节量气装置两边液面相平,读数、列式计算.
问题讨论:(1)⑥中调节两边液面相平的方法是:将水准管慢慢向下(填“上”或“下”)移动;
(2)B装置量气管上方少量植物油的作用是防止二氧化碳溶于水;
(3)若其他操作均正确,仅因下列因素可使M相对原子质量的测定结果偏大的是bc(填字母序号);
a.反应前量气管水面在0刻度处,反应后仰视读数
b.样品未分解完全即停止加热
c.量气管中未加植物油
(4)该小组测得3组数据如下表所示.
测定3组数据的目的是为了减少实验误差,最终得到CO2的体积为2.240 L.
方案二:该小组中小伟设计了如图2所示的实验装置.准确称量质量为10g 的MCO3,进行实验.
【说明】碱石灰是氧化钙和氢氧化钠固体的混合物.
操作步骤:①连接好装置,检查装置的气密性 ②打开弹簧夹C,在A处通入一段时间的空气
③称量F的质量 ④关闭弹簧夹C,滴加稀硫酸反应
⑤打开弹簧夹C,再次通入一段时间空气
⑥再次称量F的质量,得前后两次质量差为4.4g.
问题探究:(1)E、G装置的作用分别是吸收产生气体中的水分、防止空气中的水蒸气和二氧化碳进入F中.若没有G装置,则测定的M的相对原子质量会偏大(填“偏大”、“偏小”、“不变”).
(2)实验选用稀硫酸而不选用稀盐酸的理由是使用稀盐酸会使产生的二氧化碳中混有氯化氢气体,导致测定结果不准确.
(3)下列措施可以提高实验结果准确性的是abc
a.②⑤步骤中通入空气时都要缓缓通入 b.④步骤中滴加稀硫酸时要慢慢滴入
c.滴加稀硫酸要过量,直至D中没有气泡产生
(4)根据实验数据,求MCO3中金属M的相对原子质量(写出计算过程)

方案一:该小组中小梅设计如图1实验装置及步骤(友情提醒:MCO3═MO+CO2↑)
操作步骤:
①连接装置并检查装置的气密性;
②准确称量质量为10g 的MCO3;
③装好药品并调节量气装置两边液面相平,读数;
④加热至样品质量不再减少;
⑤冷却到室温;
⑥再次调节量气装置两边液面相平,读数、列式计算.
问题讨论:(1)⑥中调节两边液面相平的方法是:将水准管慢慢向下(填“上”或“下”)移动;
(2)B装置量气管上方少量植物油的作用是防止二氧化碳溶于水;
(3)若其他操作均正确,仅因下列因素可使M相对原子质量的测定结果偏大的是bc(填字母序号);
a.反应前量气管水面在0刻度处,反应后仰视读数
b.样品未分解完全即停止加热
c.量气管中未加植物油
| 组别 | 样品质量 | CO2体积 |
| 第1组 | 10g | 2.239L |
| 第2组 | 10g | 2.241L |
| 第3组 | 10g | 2.240L |
测定3组数据的目的是为了减少实验误差,最终得到CO2的体积为2.240 L.
方案二:该小组中小伟设计了如图2所示的实验装置.准确称量质量为10g 的MCO3,进行实验.
【说明】碱石灰是氧化钙和氢氧化钠固体的混合物.
操作步骤:①连接好装置,检查装置的气密性 ②打开弹簧夹C,在A处通入一段时间的空气
③称量F的质量 ④关闭弹簧夹C,滴加稀硫酸反应
⑤打开弹簧夹C,再次通入一段时间空气
⑥再次称量F的质量,得前后两次质量差为4.4g.
问题探究:(1)E、G装置的作用分别是吸收产生气体中的水分、防止空气中的水蒸气和二氧化碳进入F中.若没有G装置,则测定的M的相对原子质量会偏大(填“偏大”、“偏小”、“不变”).
(2)实验选用稀硫酸而不选用稀盐酸的理由是使用稀盐酸会使产生的二氧化碳中混有氯化氢气体,导致测定结果不准确.
(3)下列措施可以提高实验结果准确性的是abc
a.②⑤步骤中通入空气时都要缓缓通入 b.④步骤中滴加稀硫酸时要慢慢滴入
c.滴加稀硫酸要过量,直至D中没有气泡产生
(4)根据实验数据,求MCO3中金属M的相对原子质量(写出计算过程)
