题目内容
7.实验室有一包固体粉末,可能由CaCO3、CaO、Na2CO3中的一种或几种组成,为确定其组成,实验员取少量该固体粉末样品进行以下实验: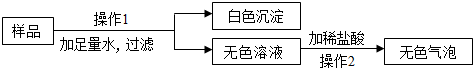
请回答:
(1)根据实验可以确定白色沉淀是CaCO3(填化学式);操作2完成后的溶液中一定含有的溶质是NaCl(填化学式).
(2)原固体粉末可能组成有3种情况.
(3)小明取一定量的CaCO3、CaO、Na2CO3粉末混合组成样品倒入试管,重复以上实验,却与以上现象不完全相同,他的操作没有失误之处,请指出现象不同之处是加入盐酸后开始没有气泡,待一段时间后产生气泡,原因是如果碳酸钠过量时,加入盐酸先与氢氧化钠反应,把氢氧化钠反应完再与碳酸钠反应,所以反应一段时间后再产生气泡.
分析 把固体粉末加入水中,得到白色沉淀,根据题给的物质可以判断该白色沉淀为碳酸钙,得到的无色溶液与可以与稀盐酸反应生成无色气体,可以判断在无色溶液中含有碳酸钠,可以据此分析原固体粉末中一定含有碳酸钠,白色沉淀的产生可能是原有的,也可能是反应产生的进行组合即可.
解答 解:将白色粉末加入足量水后产生白色沉淀,可知该白色沉淀应该为碳酸钙,得到的无色溶液能够和稀盐酸反应生成气体,可以知道在固体粉末中一定含有碳酸钠,而白色沉淀碳酸钙可能是混合物中含有的,结合氧化钙可以和水反应生成氢氧化钙这一知识点,可以判断白色沉淀也可能是碳酸钠与氢氧化钙发生了反应而生成的,所以碳酸钙和氧化钙都为可能含有的物质;
(1)白色沉淀是碳酸钙,操作2完成后的溶液中一定含有的溶质是氯化钠,故填:CaCO3;NaCl;
(2)白色粉末的可能组合为:①碳酸钠,氧化钙; ②碳酸钠,碳酸钙; ③碳酸钠,氧化钙,碳酸钙等三种可能的组成.故有3种情况,故填:3;
(3)可以从放入盐酸后气泡产生的时间以及是否有气体生成的方面分析,重点是对放入物质量的角度讨论,如:加入盐酸后开始没有气泡,待一段时间后产生气泡;如果碳酸钠过量时,加入盐酸先与氢氧化钠反应,把氢氧化钠反应完再与碳酸钠反应,所以反应一段时间后再产生气泡(或没有气泡产生;如果碳酸钠没有过量时,加入盐酸后不会产生气泡或加入盐酸的量少,导致盐酸先和氢氧化钠反应没有气泡).故填:加入盐酸后开始没有气泡,待一段时间后产生气泡;如果碳酸钠过量时,加入盐酸先与氢氧化钠反应,把氢氧化钠反应完再与碳酸钠反应,所以反应一段时间后再产生气泡.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
18.“绿色化学“要求从根本上消灭污染,它包括“原料的绿色化““化学反应的绿色化““产物的绿色化“等内容.其中“化学反应的绿色化“要求原料物质中所有的原子完全被利用且全部转入期望的产品中.下列符合“化学反应的绿色化“的是( )
| A. | 化工厂用氨、二氧化碳和水制碳酸氢铵:NH3+H2O+CO2=NH4HCO3 | |
| B. | 实验室用石灰石和稀盐酸反应制取二氧化碳:CaCO3+2HCl=CaCl2+CO2↑+H2O | |
| C. | 氯化铵与消石灰混合研磨产生氨气:2NH4C1+Ca(OH)2=CaCl2+2NH3↑+2H2O | |
| D. | 氢化钙(CaH2)与水反应可以得到氢气:CaH2+2H2O=Ca(OH)2+2H2↑ |
12.如图是初中化学中实验室制取气体的两种基本装置和三种常用的收集方法,请比较装置A和装置B的差异:
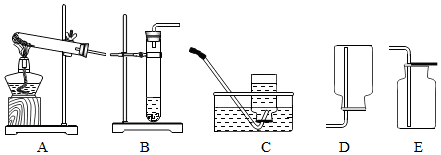

| 装置A | 装置B | |
| 反应状态 | 固体反应生成气体 | 固体和液体反应生成气体 |
| 反应条件 | 加热 | 无需加热 |
 MgO
MgO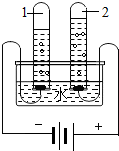 水是生命的源泉,也是不可缺少的资源.
水是生命的源泉,也是不可缺少的资源.