题目内容
14.已知碳14原子中,原子核内含有6个质子和8个中子,则碳14原子核外电子数为( )| A. | 6 | B. | 8 | C. | 12 | D. | 14 |
分析 根据在原子中,原子序数=质子数=核电荷数=核外电子数,进行解答.
解答 解:在原子中,原子序数=质子数=核电荷数=核外电子数,碳14的原子中,原子核内含有6个质子,因此原子核外电子数为6.
故选A.
点评 注意:原子序数=质子数=核电荷数=核外电子数的前提条件是在原子中.

练习册系列答案
相关题目
4.关于燃烧、爆炸、自燃、缓慢氧化的共同点是( )
①都发光 ②都放热 ③都很激烈 ④都是氧化反应.
①都发光 ②都放热 ③都很激烈 ④都是氧化反应.
| A. | ①② | B. | ①③ | C. | ②④ | D. | ①②③④ |
5. M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动.
M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动.
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;你的猜想是M>Al>Cu.
【设计与实验一】小莉取M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如表的实验(试管中均盛有体积相同、溶质质量分数也相同的稀盐酸);
【交流与表达】同学们对同一实验得出两种不同结论的现象进行了讨论,明白了实验刚开始时试管③中无气泡产生的原因,该原因是铝表面有一层氧化膜.
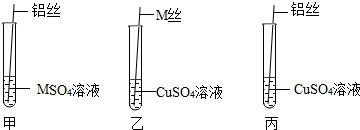
【设计与实验二】为了进一步探究三种金属的活动性顺序,同学们取粗细相同,打磨干净的M丝、铝丝及相关溶液,又进行了如图所示的实验:
(1)试管乙中观察到的现象是M表面出现一层红色物质.
(2)试管丙中反应的化学方程式为2Al+3CuSO4=Al2(SO4)3+3Cu.
【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管丙(填试管编号)中的实验,也可以得出正确的结论.
【解释与结论】通过以上实验,同学们得出了三种金属的活动性顺序.
【评价与反思】实验结束后,同学们对实验过程进行了如下反思:
(1)影响金属与酸反应速率快慢的因素,除了相互反应的金属和酸的性质外,还有反应物接触面积、温度(任写一种)
(2)探究金属活动性顺序时,除了上述实验中已经用到的两种方法外,还可以根据与氧气反应的剧烈程度进行判断(任写一种)
 M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动.
M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动.【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;你的猜想是M>Al>Cu.
【设计与实验一】小莉取M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如表的实验(试管中均盛有体积相同、溶质质量分数也相同的稀盐酸);
| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| 刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu:M>Al |
| 几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 | Al>M>Cu |
【设计与实验二】为了进一步探究三种金属的活动性顺序,同学们取粗细相同,打磨干净的M丝、铝丝及相关溶液,又进行了如图所示的实验:
(1)试管乙中观察到的现象是M表面出现一层红色物质.
(2)试管丙中反应的化学方程式为2Al+3CuSO4=Al2(SO4)3+3Cu.
【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管丙(填试管编号)中的实验,也可以得出正确的结论.
【解释与结论】通过以上实验,同学们得出了三种金属的活动性顺序.
【评价与反思】实验结束后,同学们对实验过程进行了如下反思:
(1)影响金属与酸反应速率快慢的因素,除了相互反应的金属和酸的性质外,还有反应物接触面积、温度(任写一种)
(2)探究金属活动性顺序时,除了上述实验中已经用到的两种方法外,还可以根据与氧气反应的剧烈程度进行判断(任写一种)
2.在含有大量 Mg2+、H+、SO42-的溶液中,还可以大量存在的是( )
| A. | NO3- | B. | Ba2+ | C. | OH- | D. | CO32- |
19.高铁酸钾(K2FeO4)是一种集吸附、凝聚、杀菌等功能为一体的新型高效水处理剂,可将水中的三氯乙烯(C2HCl3)除去85.6%,下列说法正确的是( )
| A. | K2FeO4是氧化物 | |
| B. | C2HCl3中三种元素的质量比是2:1:3 | |
| C. | K2FeO4中Fe元素的化合价为+3价 | |
| D. | 三氯乙烯中碳元素的质量分数约为18.25% |
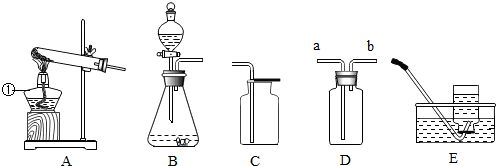
6.小明同学设计以下实验来探究可燃物燃烧的条件和测定空气中氧气的含量.(已知:白磷的着火点是40℃,红磷的着火点是240℃)
(1)实验过程②是向烧杯中加入适量的冷水,烧杯中发生反应的化学方程式为CaO+H2O═Ca(OH)2;
(2)白磷燃烧反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(3)根据实验2的结果,计算空气中氧气的体积分数约为$\frac{60mL}{350mL-50mL}$=$\frac{1}{5}$(写出计算式和结果);
(4)在整个实验2的过程中,集气瓶内的压强变化是先变大后变小到与大气压相等,集气瓶中预先装入50mL水,水起的作用是吸收白烟,同时防止集气瓶内的空气因瓶内温度升高、压强增大而逸散到瓶外.
| 实验装置 | 实验过程 | 实验现象 |
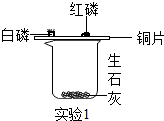 | ①取一烧杯,加入适量的生石灰,再分别取少量白磷、红磷放在烧杯上的铜片上. ②… | 一会儿白磷发生燃烧,红磷不燃烧 |
 | ③先在容积为350mL的集气瓶中装进50mL滴有红墨水的水,在燃烧匙中放足量白磷,量筒中盛入足量水. ④按图连好仪器,用激光手电照射白磷,白磷燃烧. | 集气瓶和量筒中的水均为红色,量筒内的液体体积减少约60mL |
(2)白磷燃烧反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(3)根据实验2的结果,计算空气中氧气的体积分数约为$\frac{60mL}{350mL-50mL}$=$\frac{1}{5}$(写出计算式和结果);
(4)在整个实验2的过程中,集气瓶内的压强变化是先变大后变小到与大气压相等,集气瓶中预先装入50mL水,水起的作用是吸收白烟,同时防止集气瓶内的空气因瓶内温度升高、压强增大而逸散到瓶外.
3.下列化肥属于磷肥的是( )
| A. | Ca3(PO4)2 | B. | KNO3 | C. | CO(NH2)2 | D. | (NH4)2SO4 |
17.下列有关资源、能源的叙述错误的是( )
| A. | 海洋是巨大的资源宝库,其中海洋约占地球表面的71% | |
| B. | 太阳能、风能、地热能等的利用,解决了化石能源面临耗尽的问题,并在一定程度上减少了对环境的污染 | |
| C. | 现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%--40% | |
| D. | 有石油的地方一定有天然气存在 |