题目内容
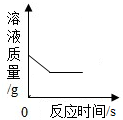
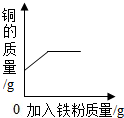
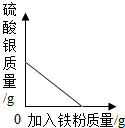
17.现有实验室制取二氧化碳的废液,其中主要含有HCl与CaCl2,为了分析废液中HCl和CaCl2的质量分数,进行了如图所示实验:
请根据实验所得数据进行计算:
(1)产生二氧化碳气体的质量为4.4g.
(2)废液中CaCl2的质量分数.
分析 (1)根据盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,二氧化碳和氢氧化钠反应,氢氧化钠溶液增加的质量为二氧化碳的质量解答;
(2)根据产生沉淀的质量,结合氯化钙和碳酸钠反应方程式计算废液中氯化钙的质量;
解答 解:
(1)盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,二氧化碳和氢氧化钠反应,氢氧化钠溶液增加的质量为二氧化碳的质量为4.4g;
(2)盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,盐酸被消耗完,氯化钙与碳酸钠反应,生成沉淀,
观察图可知:废液中的氯化钙与碳酸钠最多反应生成20g碳酸钙
设氯化钙的质量为x,
Na2CO3+CaCl2═CaCO3↓+2NaCl
111 100
x 20g
$\frac{111}{x}=\frac{100}{20g}$
x=22.2g
废液中CaCl2的质量分数=$\frac{22.2g}{100g}×$100%=22.2%
答案:
(1)4.4
(2)废液中CaCl2的质量分数22.2%
点评 本题主要考查化学反应中的物质成分的探究,解题时要结合复分解反应的原理和反应物的过量问题进行分析,此外还考查了含杂质物质的化学方程式计算和反应后溶质质量的计算,要结合反应原理和图象细致分析,难度较大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
8.有氧化铁和氧化亚铁的混合物,已知混合物中铁的质量分数为77%.则混合物中氧化亚铁的质量分数为( )
| A. | 10% | B. | 30% | C. | 55% | D. | 90% |
12.用固体氯化钠配制50g质量分数为5%的氯化钠溶液,在①溶解,②称量并转移,③量取并转移,④计算等操作步骤中,先后顺序正确的是( )
| A. | ①②③④ | B. | ④③①② | C. | ④②③① | D. | ④②①③ |







 如图是实验室制取并探究二氧化碳性质的装置:
如图是实验室制取并探究二氧化碳性质的装置: