题目内容
16.研究发现一种带螺纹的矿石能在氧气中燃烧,主要反应是4X+11O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3+8SO2.下列有关说法中不正确的是( )| A. | X的化学式是FeS2 | B. | Fe2O3中铁元素的质量分数为70% | ||
| C. | 反应前后氧元素的化合价发生改变 | D. | 生成的SO2是产生温室效应的气体 |
分析 A、化学反应前后,元素的种类不变,原子的种类、总个数不变;
B、根据物质的化学式可以计算组成元素的质量分数;
C、单质中元素的化合价为零,化合物中元素的化合价代数和为零;
D、生成的SO2不是产生温室效应的气体.
解答 解:A、由4X+11O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3+8SO2可知,每个X中含有1个铁原子和2个硫原子,是二硫化亚铁,化学式是FeS2,该选项说法正确;
B、Fe2O3中铁元素的质量分数为:$\frac{112}{160}$×100%=70%,该选项说法正确;
C、反应前氧元素的化合价是0,反应后氧元素的化合价是-2,该选项说法正确;
D、生成的SO2不是产生温室效应的气体,错误.
故选D.
点评 单质中,因为没有元素之间的化合,所以规定单质中元素的化合价为零;
化合物中,元素的化合价代数和为零,这是判断物质的化学式或元素化合价是否正确的依据.

练习册系列答案
相关题目
6.如图是某化学反应的微观示意图,下列说法中正确的是( )


| A. | 该反应属于置换反应 | |
| B. | 反应中甲、乙的质量比为17﹕32 | |
| C. | 甲物质含有4个原子 | |
| D. | 反应物中只有一种元素的化合价改变 |
1.我国女药学家、诺贝尔奖获得者屠呦呦发现的青蒿素(化学式为C15H22O5)是一种用于治疗疟疾的药物.下列有关青蒿素的说法不正确的是( )
| A. | 青蒿素属于有机物 | |
| B. | 青蒿素分子中碳、氢、氧的原子个数比为15:22:5 | |
| C. | 青蒿素的相对分子质量282g | |
| D. | 青蒿素由碳、氢、氧三种元素组成 |
8.近年来全国多个城市均遭遇了雾霾来袭,下列不可能是雾霾产生的原因的是( )
| A. | 焚烧秸秆 | B. | 汽车尾气 | C. | 光合作用 | D. | 燃烧煤炭 |
5.下列有关微粒的说法正确的是( )
| A. | 原子通过得失电子形成离子,但离子不能形成原子 | |
| B. | 由分子构成的物质发生化学变化时,分子本身没有改变 | |
| C. | 过氧化氢是由氢原子和氧原子构成的,它与水的组成元素相同 | |
| D. | 原子、分子、离子都是构成物质的微粒,构成物质的微粒在不停地运动 |
6.肥皂是生活中常见的用品.其主要成分为硬脂酸钠(C17H35COONa).下列有关硬脂酸钠的说法不正确的是( )
| A. | 硬脂酸钠属于盐 | |
| B. | 由一种金属元素和三种非金属元素组成 | |
| C. | 钠元素的化合价为+1 | |
| D. | 硬脂酸钠碳、氢、氧三种元素的原子个数比是17:35:2 |
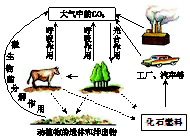 自然界就是一个天然“工厂”.自然界中的物质循环,形成了自然界中物质的平衡.如图所示为自然界中碳循环的示意.
自然界就是一个天然“工厂”.自然界中的物质循环,形成了自然界中物质的平衡.如图所示为自然界中碳循环的示意.