题目内容
实验室现有高锰酸钾、稀硫酸、稀盐酸、石灰石、棉花及以下仪器:

(1)利用上述药品实验室制取并收集氧气所需要的仪器是________(填序号);制取该气体的化学方程式为 ________。
(2)请写出实验室制取二氧化碳的化学方程式:________
(3)下图甲、乙、丙分别为CO2气体的制取、干燥、验证装置,则乙装置所装试剂是________。请在下图虚框中将乙装置直接补画完整,并将甲、乙、丙连接成完整的实验装置图________。

(4)实验过程中丙装置内的实验现象是________。由此得出的结论是________。
①③⑤⑥⑦⑧ 2KMnO4K2MnO4 + MnO2 + O2↑ CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ 浓硫酸 燃着的蜡烛由下至上依次熄灭 二氧化碳的密度比空气的密度大,且不支持燃烧 【解析】(1)高锰酸钾、稀硫酸、稀盐酸、石灰石、棉花中只有高锰酸钾可以制取氧气,而且需要加热。氧气的密度大于空气的密度并不易溶于水,我们据此选择制取氧气的装置;并根据反应物和反应...
练习册系列答案
相关题目
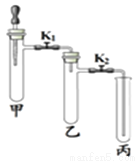
利用表中装置进行下列实验。
实验装置 | 实验1 | 实验2 |
| ①甲试管中放入少量MnO2,滴管中放入过氧化氢溶液,乙、丙中分别放入一小块白磷依次加入适量80℃的水,白磷均不燃烧 ②打开K1、K2,将过氧化氢溶液滴入试管,观察到乙试管中白磷不燃烧,丙中白磷燃烧 ③一段时间后,丙中导管内液 面上升 | ①关闭K1,打开K2,甲试管中充满CO2,滴管中放入浓NaOH溶液;乙试管中放入适量铁粉,丙中放入约半试管稀盐酸 ②将浓NaOH溶液滴入甲试管中,一段时间后,打开K1 ③一段时间后,观察乙、丙试管中的现象 |
(1)实验1:甲中发生反应的化学方程式是_______________,对比乙和丙中的实验现象,本实验欲探究的燃烧条件是_____________;步骤③中“丙中导管内液面上升”的原因是________________。
(2)实验2:甲中发生反应的化学方程式为____________;步骤③乙中的现象是_____________;丙试管中的现象是_________。
2H2O22H2O+O2↑ 可燃物燃烧需要与氧气接触 甲中反应放热,一段时间后温度降低,导致压强减小 CO2+2NaOH==Na2CO3+H2O 丙试管中稀盐酸被倒吸入乙试管,产生大量气泡,溶液由无色变为浅绿色 开始丙试管中稀盐酸被倒吸入,稍后有气泡产生 【解析】本题主要考查碱、酸的性质,燃烧条件的探究。解答时要根据各种物质的性质,气体压强的知识,结合各方面条件进行分析、判断,从而得出正确的...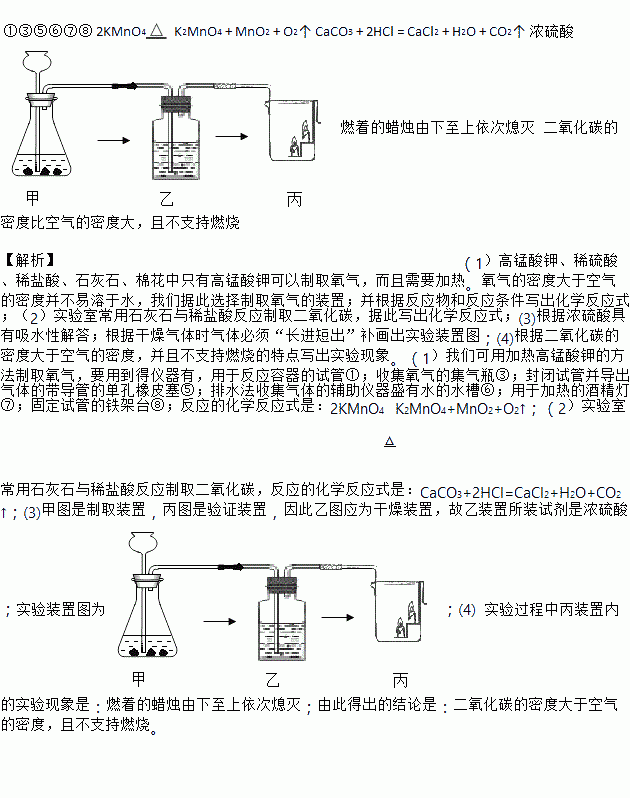

 n 的值为___________;
n 的值为___________;