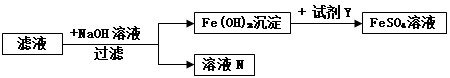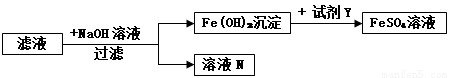题目内容
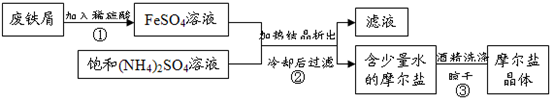
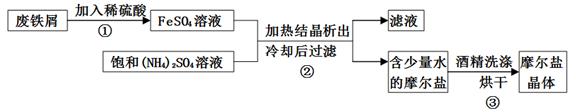
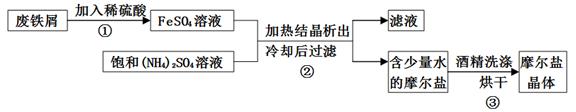
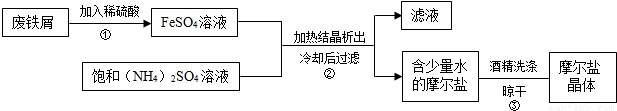
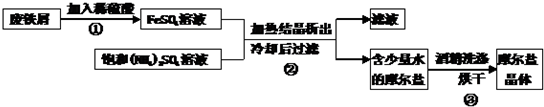
摩尔盐(硫酸亚铁铵晶体)具有重要用途,下图为制取摩尔盐过程的示意图.请回答下列问题:
(1)实验前,先用碳酸钠溶液浸泡废铁屑表面油渍.碳酸钠溶液可除去油渍是因为碳酸钠溶液的pH
(2)废铁屑的主要成分是铁,同时含有少量氧化铁.步骤①中有多个化学反应,请写出其中2个反应的化学方程式:
(3)根据步骤③可知,摩尔盐
(4)步骤②所得滤液含有未反应的FeSO4、(NH4)2SO4,可采用如下流程回收利用.
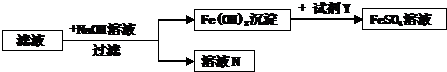
滤液N中一定含有的溶质是

(1)实验前,先用碳酸钠溶液浸泡废铁屑表面油渍.碳酸钠溶液可除去油渍是因为碳酸钠溶液的pH
>
>
7(填“>”、“<”或“=”).(2)废铁屑的主要成分是铁,同时含有少量氧化铁.步骤①中有多个化学反应,请写出其中2个反应的化学方程式:
Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
.(3)根据步骤③可知,摩尔盐
不能
不能
溶解于酒精(填“能”或“不能”).(4)步骤②所得滤液含有未反应的FeSO4、(NH4)2SO4,可采用如下流程回收利用.

滤液N中一定含有的溶质是
硫酸钠
硫酸钠
,试剂Y是硫酸(或H2SO4)
硫酸(或H2SO4)
.分析:碱性溶液能溶解油污,铁、氧化铁都能与稀硫酸反应;亚铁离子与氢氧根离子能结合成氢氧化亚铁沉淀,铵根离子能与氢氧根离子结合成氨气和水;能与酒精洗涤摩尔盐,说明摩尔盐不溶于酒精.
解答:解:(1)碱性溶液能溶解油污,故碳酸钠溶液pH大于7;
(2)废铁屑中有铁、氧化铁,铁与稀硫酸反应生成硫酸亚铁和氢气,氧化铁和稀硫酸反应生成硫酸铁和水,铁还能与硫酸铁反应生成硫酸亚铁,方程式为Fe+H2SO4═FeSO4+H2↑; 3H2SO4+Fe2O3═Fe2(SO4)3+3H2O;Fe2(SO4)3+Fe═3FeSO4
(3)根据步骤③可知,用酒精可以洗去摩尔盐表面的水,然后晾干,说明摩尔盐不溶于酒精;
(4)氢氧化铁与Y反应只生成硫酸亚铁,故Y是硫酸,滤液中含有硫酸亚铁,硫酸铵,硫酸亚铁与氢氧化钠反应生成氢氧化亚铁沉淀和硫酸钠,硫酸铵与氢氧化钠反应生成硫酸钠、氨气和水,溶液N中一定含有硫酸钠.
故答案为:(1)>;(2)Fe+H2SO4=FeSO4+H2↑;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O (两个化学方程式的顺序可颠倒); (3)不能; (4)硫酸钠(或Na2SO4);硫酸(或H2SO4).
(2)废铁屑中有铁、氧化铁,铁与稀硫酸反应生成硫酸亚铁和氢气,氧化铁和稀硫酸反应生成硫酸铁和水,铁还能与硫酸铁反应生成硫酸亚铁,方程式为Fe+H2SO4═FeSO4+H2↑; 3H2SO4+Fe2O3═Fe2(SO4)3+3H2O;Fe2(SO4)3+Fe═3FeSO4
(3)根据步骤③可知,用酒精可以洗去摩尔盐表面的水,然后晾干,说明摩尔盐不溶于酒精;
(4)氢氧化铁与Y反应只生成硫酸亚铁,故Y是硫酸,滤液中含有硫酸亚铁,硫酸铵,硫酸亚铁与氢氧化钠反应生成氢氧化亚铁沉淀和硫酸钠,硫酸铵与氢氧化钠反应生成硫酸钠、氨气和水,溶液N中一定含有硫酸钠.
故答案为:(1)>;(2)Fe+H2SO4=FeSO4+H2↑;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O (两个化学方程式的顺序可颠倒); (3)不能; (4)硫酸钠(或Na2SO4);硫酸(或H2SO4).
点评:本题看上去是一道新信息题,但题目考查的知识点都是课本基础知识,熟练掌握酸碱盐的化学性质即可解答本题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目