题目内容
5.化学上常用燃烧法测定有机物的组成.现取2.3g某有机物在氧气中充分燃烧生成4.4gCO2和2.7gH2O,下列说法正确的是( )| A. | 该有机物中只含有碳、氢两种元素 | |
| B. | 实验中所消耗氧气的质量为4.8g | |
| C. | 该有机物中碳、氢元素的质量比为6:1 | |
| D. | 该有机物可能为乙烯(C2H4) |
分析 根据有机物燃烧生成二氧化碳和水可知有机物中一定含有C、H两种元素,利用4.4g二氧化碳和2.7g水可求C、H两种元素的质量,若C、H两种元素的质量等于2.3g,则有机物不含有O元素,若C、H两种元素的质量小于2.3g,则有机物中含有O元素.
解答 解:A、由2.3g某有机物在足量的氧气中充分燃烧,生成4.4g二氧化碳和2.7g水,则有机物中一定含有C、H两种元素,
C元素的质量为4.4g×$\frac{12}{44}$×100%=1.2g,
H元素的质量为2.7g×$\frac{2}{18}$×100%=0.3g,
1.2g+0.3g=1.5g<2.3g,
则有机物中一定含有O元素,且O元素的质量为2.3g-1.5g=0.8g,所以有机物中只含有碳、氢、氧三种元素,故说法错误.
B、根据质量守恒定律,实验中用去氧气的质量为4.4g+2.7g-2.3g=4.8g,故说法正确;
C、该有机物中碳、氢元素的质量比为1.2g:0.3g=4:1,故说法错误;
D、该有机物中只含有碳、氢、氧三种元素,不可能为乙烯(C2H4),故说法错误;
故选:B.
点评 本题是运用化学中的基本思想质量守恒思想,通过归纳不同物质或不同变化过程中相同点和不同点有效地寻找出它们之间的内在联系以及融合点和嫁接点,从而培养了学生的创新思维能力.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
15.下列有关物质性质叙述正确的是( )
| A. | CO2、CO组成相同,故密度相同 | |
| B. | H2SO4溶液能使紫色石蕊试液变红 | |
| C. | 已知NaHSO4溶液呈酸性,故该物质属于酸 | |
| D. | 向稀硫酸中加入少量Ag粉,会有气泡生成 |
13.下列生活事例中,属于化学变化的是( )
| A. | 西瓜榨汁 | B. | 铁锅生锈 | C. | 冰雪消融 | D. | 白醋挥发 |
20.吸烟有害健康,非吸烟者在很多场合往往被动吸烟,这是因为( )
| A. | 分之间有间隔 | |
| B. | 分子的质量和体积都很小 | |
| C. | 分子在不断运动 | |
| D. | 分子是保持物质化学性质的最小粒子 |
14.闪电时空气中有臭氧(O3)生成,3O2$\frac{\underline{\;无声放电\;}}{\;}$2O3下列说法正确的是( )
| A. | 氧气与臭氧相互转化是物理变化 | |
| B. | 氧气与臭氧化学性质相同 | |
| C. | ag质量的氧气完全转化成臭氧,其质量也是ag | |
| D. | 氧气与臭氧都属于氧化物 |
17.下列措施是为了防止臭氧层被进一步破坏的是( )
| A. | 食用加碘食盐 | B. | 使用无磷洗衣粉 | C. | 使用无氟冰箱 | D. | 使用无铅汽油 |
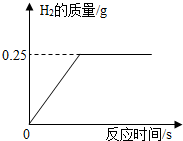 硅钢合金是变压器、充电器中的核心材料,其主要成份是铁和硅.向8.4g硅钢中加入100g稀硫酸,恰好完全反应(硅及其杂质不溶于水,且都不与稀硫酸反应),放出气体的质量与反应时的关系如图所示.
硅钢合金是变压器、充电器中的核心材料,其主要成份是铁和硅.向8.4g硅钢中加入100g稀硫酸,恰好完全反应(硅及其杂质不溶于水,且都不与稀硫酸反应),放出气体的质量与反应时的关系如图所示.