题目内容
2.根据可燃物燃烧的条件分析,灭火可从两个方面采取措施:一是降低温度至着火点以下,二是隔绝空气.
分析 根据可燃物燃烧的两个条件及破坏燃烧的条件就能达到灭火的措施进行分析.
解答 解:根据燃烧的条件可知,物质燃烧必须具有可燃性(可燃物),必须与氧气或空气接触,温度必须达到燃烧所需的最低温度即着火点,这三个条件缺一不可.所以灭火可从两个方面采取措施是:降低温度至着火点以下或隔绝空气.
故答案为:降低温度至着火点以下;隔绝空气.
点评 本题难度不大,掌握燃烧的条件(具有可燃性、与氧气接触、达到着火点,这三个条件缺一不可)及灭火的措施是解题的关键.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
13.中学生应有一定的安全常识,下列做法不合理的是( )
| A. | 夜间发现液化石油气泄漏,应先关掉气瓶的阀门并开窗通风,才开灯检查 | |
| B. | 烧碱溶液不小心溅入眼睛,应该用稀盐酸溶液冲洗 | |
| C. | 在实验室不小心碰倒酒精灯后酒精燃烧起来,应该用湿布盖灭 | |
| D. | 发生火灾时被困火灾区,应该用湿毛巾捂住口鼻并尽量贴着地面逃离 |
10.下列实验操作,正确的是( )
| A. | 直接把食盐放在托盘天平上称量 | |
| B. | 制取氧气时,连接好仪器后就加入药品进行实验 | |
| C. | 振荡时,手指堵住试管口,上下晃动 | |
| D. | 连接仪器时,先将玻璃管湿润,再缓缓旋转插入胶塞 |
7.化学实验重要而有趣,请根据你掌握的知识来判断以下实验操作,正确的是( )
| A. | 用镊子夹取粉末状固体 | |
| B. | 用燃着的酒精灯去点燃另一盏酒精灯 | |
| C. | 实验用剩的药品要放回原瓶,以免浪费药品 | |
| D. | 实验要求中未说明药品的用量,就应取最少量,液体1-2mL,固体盖满试管底部 |
14.某混合气体由H2、CO、CO2组成,为了验证三种气体的存在,进行了下列实验操作(如图所示):
(捉示:H2、CO不与澄清石灰水、氢氧化钠溶液、浓硫酸反应,CO燃烧后生成CO2.
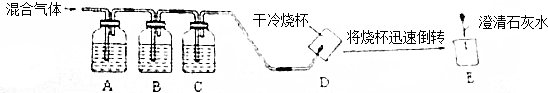
(1)请分析上图所示装置的实验象理,填写下列表中的空格:
(2)实验证明该混合气体中含有H2、CO、CO2.
能证明H2存在的现象是干燥的烧杯内壁有水雾生成.
能证明CO存在的现象是E中澄清的石灰水便浑浊.
能证明CO2存在的现象是A中澄清的石灰水便浑浊.
(捉示:H2、CO不与澄清石灰水、氢氧化钠溶液、浓硫酸反应,CO燃烧后生成CO2.

(1)请分析上图所示装置的实验象理,填写下列表中的空格:
| 仪器编号 | 所盛试剂的名称 | 试剂或装置的作用 |
| A | 澄清石灰水 | 检验CO2气体 |
| B | 氢氧化钠溶液 | 除去CO2气体 |
| C | 浓硫酸 | 吸收水蒸气 |
| D | 检验H2气体 | |
| E | 检验CO气体 |
能证明H2存在的现象是干燥的烧杯内壁有水雾生成.
能证明CO存在的现象是E中澄清的石灰水便浑浊.
能证明CO2存在的现象是A中澄清的石灰水便浑浊.
12.小明发现一种淡黄色的粉末可以用于杀菌、消毒和漂白.
【定性探究】探究该固体的成分.
【提出问题】该淡黄色固体的化学成分是什么?
【查阅资料】(1)硫单质是一种淡黄色固体,难溶于水,在空气中点燃硫单质,生成一种无色、有刺激性气味的气体.
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热.
【设计实验方案】
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象.
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象.
比较以上两方案,你认为的最佳方案是方案一,理由是(从环保或操作角度分析)该操作简单,无污染,现象明显.
【实验验证并得出结论】小明向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH).通过实验验证,确定该淡黄色粉末为过氧化钠.
小明想对生成的气体成分判断,他提出了以下两种假设:①该气体是CO ②该气体是O2你认为上述假设哪个更合理①(填“①”或“②”).理由是不符合质量守恒定律,反应物中没有碳元素.
请设计一个实验,验证合理假设(写出简要操作步骤、实验现象和结论).
【分析】过氧化钠与水反应的符号表达式为2Na2O2+2H2O═4NaOH+O2↑.
【定量探究】78克过氧化钠与多少克二氧化碳中所含氧元素的质量相等?(列式计算)
【定性探究】探究该固体的成分.
【提出问题】该淡黄色固体的化学成分是什么?
【查阅资料】(1)硫单质是一种淡黄色固体,难溶于水,在空气中点燃硫单质,生成一种无色、有刺激性气味的气体.
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热.
【设计实验方案】
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象.
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象.
比较以上两方案,你认为的最佳方案是方案一,理由是(从环保或操作角度分析)该操作简单,无污染,现象明显.
【实验验证并得出结论】小明向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH).通过实验验证,确定该淡黄色粉末为过氧化钠.
小明想对生成的气体成分判断,他提出了以下两种假设:①该气体是CO ②该气体是O2你认为上述假设哪个更合理①(填“①”或“②”).理由是不符合质量守恒定律,反应物中没有碳元素.
请设计一个实验,验证合理假设(写出简要操作步骤、实验现象和结论).
| 操作步骤 | 实验现象 | 结论 |
| 取少量固体粉末于试管中,向试管中加入2mL水,将带火星的木条伸入试管中 | 木条复燃 | 该气体为氧气 |
【定量探究】78克过氧化钠与多少克二氧化碳中所含氧元素的质量相等?(列式计算)