题目内容
6.为了将混有硫酸钠、碳酸氢铵的氯化钠提纯,并制得纯净的氯化钠溶液,某学生设计如下实验:
(1)操作②能否用硝酸钡溶液?不能,.理由是用硝酸钡会引入新杂质NO${\;}_{3}^{-}$.
(2)进行操作②后,如何判断SO${\;}_{4}^{2-}$已除尽,方法是取少量上层澄清溶液,再滴加BaCl2溶液,如无沉淀出现则说明SO${\;}_{4}^{2-}$已除尽,反之则有.
(3)操作③的目的是除去过量的Ba2+;为什么不先过滤而后加碳酸钠溶液,其理由是一次性过滤掉BaSO4沉淀和BaCO3沉淀.
(4)此设计方案是否严密,如不严密,说明如何改进在操作④之后应加过量盐酸以除去Na2CO3,然后再加热煮沸除去HCl.
分析 (1)除杂时不能引入新的杂质;
(2)加入氯化钡溶液检验硫酸根离子是否除尽;
(3)加入碳酸钠溶液,除去过量的氯化钡,根据过滤实验用到的仪器进行回答;
(4)除杂时,氯化钠溶液中不能有其他杂质.
解答 解:(1)加入硝酸钠溶液,硝酸钠和硫酸钠反应生成硫酸钡和硝酸钠,除去了硫酸钠,但引入了硝酸钠等新的杂质,故答案为:不能,用硝酸钡会引入新杂质NO${\;}_{3}^{-}$;
(2)加入过量氯化钡溶液除去硫酸根离子,检验硫酸根离子已除尽,可静止片刻在上层清液处,滴加一滴氯化钡溶液,不出现浑浊就说明硫酸根离子已经除尽,故答案为:取少量上层澄清溶液,再滴加BaCl2溶液,如无沉淀出现则说明SO${\;}_{4}^{2-}$已除尽,反之则有;
(3)操作③加入碳酸钠溶液,碳酸钠与过量的氯化钡反应生成碳酸钡和氯化钠,除去过量的氯化钡,再过滤;先过滤而后加碳酸钠溶液,在加入碳酸钠溶液后生成的碳酸钡还需要过滤,一次性过滤掉BaSO4沉淀和BaCO3沉淀.故答案为:除去过量的Ba2+;一次性过滤掉BaSO4沉淀和BaCO3沉淀;
(4)此方案不严密,过量的碳酸钠没有除去,得到的溶液中含有氯化钠和过量的碳酸钠两种溶质,致使得到的氯化钠溶液不纯,应在操作④之后加入适量盐酸除去碳酸钠,然后再加热煮沸除去HCl,故答案为:在操作④之后应加过量盐酸以除去Na2CO3,然后再加热煮沸除去HCl.
点评 常见物质的分离方法和提纯是现在考试的重点和热点,可以根据所学知识进行回答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.二硫基丙醇是医疗上用于治疗砷中毒的药物,化学式为C3H8S2O,可进行肌肉注射或静脉注射.下列关于C3H8S2O的说法正确的是( )
| A. | 二硫基丙醇是氧化物 | |
| B. | 二硫基丙醇中氢元素的质量分数最大 | |
| C. | 二硫基丙醇中有3个碳原子 | |
| D. | 该物质中C、H、S、O原子的个数比为3:8:2:1 |
17.欲配制25g质量分数为10%的氯化钠溶液,下列说法不正确的是( )
| A. | 实验中用到的玻璃仪器只有烧杯和量筒 | |
| B. | 计算得氯化钠的质量为2.5g,水的体积为22.5ml | |
| C. | 量取水时,若俯视读数,会使配得的溶液浓度偏大 | |
| D. | 用天平称取该固体时将砝码和物品放反,会导致配得的溶液浓度偏小 |
14.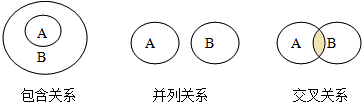 包含、并列、交叉是化学概念在逻辑上存的关系(如图示),对下概念间的关系说法正确的是( )
包含、并列、交叉是化学概念在逻辑上存的关系(如图示),对下概念间的关系说法正确的是( )
①纯净物与混合物属于包含关系;
②化合物与氧化物属于包含关系;
③单质与化合物属于交叉关系;
④金属元素与非金属元素属于并列关系;
⑤中和反应与复分解反应属于并列关系.
 包含、并列、交叉是化学概念在逻辑上存的关系(如图示),对下概念间的关系说法正确的是( )
包含、并列、交叉是化学概念在逻辑上存的关系(如图示),对下概念间的关系说法正确的是( )①纯净物与混合物属于包含关系;
②化合物与氧化物属于包含关系;
③单质与化合物属于交叉关系;
④金属元素与非金属元素属于并列关系;
⑤中和反应与复分解反应属于并列关系.
| A. | ①② | B. | ③④ | C. | ②④ | D. | ①⑤ |
11.单晶硅是制作电子集成电路的基础材料.工业上通过以下反应将自然界的二氧化硅(SiO2)转化为硅:
SiO2+2C $\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.下列分析正确的是( )
SiO2+2C $\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.下列分析正确的是( )
| A. | 二氧化硅发生了氧化反应 | B. | 碳发生了还原反应 | ||
| C. | 该反应属于分解反应 | D. | 该反应中碳是还原剂 |
18.化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
【提出问题1】该氢氧化钠溶液是否变质了呢?
【实验探究1】
【提出问题2】该氢氧化钠溶液是全部变质还是部分变质呢?
【猜想与假设]猜想1:氢氧化钠溶液部分变质. 猜想2:氢氧化钠溶液全部变质.
【查阅资料】(1)氯化钙溶液呈中性.
(2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3═CaCO3↓+2NaCl
【实验探究2】
【实验结论】该氢氧化钠溶液部分(填“部分”或“全部”)变质.
【反思与评价】
(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:2NaOH+CO2═Na2CO3+H2O.
(2)在上述【实验探究2】中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案不可行(填“可行”或“不可行”).
【理解与应用】氢氧化钠溶液容易变质,必须密封保存.实验室必须密封保存的药品还有很多,试另举一例:浓盐酸具有挥发性.
【提出问题1】该氢氧化钠溶液是否变质了呢?
【实验探究1】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡. | 有气泡冒出. | 氢氧化钠溶液一定变质了. |
【猜想与假设]猜想1:氢氧化钠溶液部分变质. 猜想2:氢氧化钠溶液全部变质.
【查阅资料】(1)氯化钙溶液呈中性.
(2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3═CaCO3↓+2NaCl
【实验探究2】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡. | 有白色沉淀生成. | 说明原溶液中一定有碳酸钠. |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液. | 溶液变红色. | 说明原溶液中一定有氢氧化钠. |
【反思与评价】
(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:2NaOH+CO2═Na2CO3+H2O.
(2)在上述【实验探究2】中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案不可行(填“可行”或“不可行”).
【理解与应用】氢氧化钠溶液容易变质,必须密封保存.实验室必须密封保存的药品还有很多,试另举一例:浓盐酸具有挥发性.
15.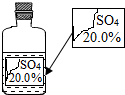 老师向同学们展示了一瓶标签受损的无色溶液(如图所示)并要求同学们进行探究:确认这瓶溶液到底是什么溶液?
老师向同学们展示了一瓶标签受损的无色溶液(如图所示)并要求同学们进行探究:确认这瓶溶液到底是什么溶液?
【提出猜想】老师提示:这瓶无色溶液只能是下列四种溶液中的一种:
①硫酸镁溶液 ②硫酸钠溶液 ③硫酸溶液 ④硫酸铵溶液
【查阅资料】Ⅰ:(NH4)2SO4的水溶液显酸性Ⅱ:常温下,相关物质的溶解度如下:
【实验探究】
Ⅰ:通过查阅资料,小明同学认为猜想②(填序号)不成立.
Ⅱ:为确定其他几种猜想是否正确,小明同学继续进行探究:
有人认为小明实验操作第二步的结论不一定正确,他的理由是硫酸铵溶液(显酸性)也能使石蕊溶液变红.
Ⅲ:请你设计实验方案,确认该溶液是硫酸溶液并完成下列实验报告:
 老师向同学们展示了一瓶标签受损的无色溶液(如图所示)并要求同学们进行探究:确认这瓶溶液到底是什么溶液?
老师向同学们展示了一瓶标签受损的无色溶液(如图所示)并要求同学们进行探究:确认这瓶溶液到底是什么溶液?【提出猜想】老师提示:这瓶无色溶液只能是下列四种溶液中的一种:
①硫酸镁溶液 ②硫酸钠溶液 ③硫酸溶液 ④硫酸铵溶液
【查阅资料】Ⅰ:(NH4)2SO4的水溶液显酸性Ⅱ:常温下,相关物质的溶解度如下:
| 物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
| 溶解度g/100g水 | 35.1 | 19.5 | 75.4 | 与水任意比互溶 |
Ⅰ:通过查阅资料,小明同学认为猜想②(填序号)不成立.
Ⅱ:为确定其他几种猜想是否正确,小明同学继续进行探究:
| 实验操作 | 实验现象 | 实验结论 |
| 第一步:若取该溶液少许于试管中,向其中滴加几滴 氢氧化钠溶液 | 溶液中有白色沉淀生成 | 猜想①成立 |
| 第二步:若用玻璃棒蘸取少许原溶液滴在pH试纸上,并跟比色卡对照 | 溶液pH小于7 | 猜想③成立 |
Ⅲ:请你设计实验方案,确认该溶液是硫酸溶液并完成下列实验报告:
| 实验操作 | 实验现象 | 实验结论 |
| 取该溶液少许于试管中,加入 锌 | 有气泡产生 | 猜想③成立,该反应的化学方程式为 Zn+H2SO4═ZnSO4+H2↑ |
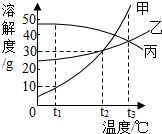 甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:
甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题: