题目内容
11.硫酸铜对过氧化氢的分解有催化作用.取8.5%的过氧化氢溶液40g倒入小烧杯中,向其中加入20%的硫酸铜溶液11.6g,使过氧化氢完全分解.计算:(1)产生氧气的质量.
(2)反应后所得溶液中硫酸铜的质量分数.
分析 (1)根据过氧化氢的质量求出氧气的质量即可;
(2)根据硫酸铜的质量然后利用溶质质量分数公式计算即可.
解答 解:(1)设生成氧气的质量为x.
2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑
68 32
40g×8.5% x
$\frac{68}{40g×8.5%\\;}=\frac{32}{x}$
x=1.6g
答:生成氧气的质量为1.6g.
(2)反应后所得硫酸铜溶液的溶质质量分数=$\frac{11.6g×20%}{40g+11.6g-1.6g}$×100%=4.64%
答:反应后所得硫酸铜溶液的溶质质量分数为4.64%.
点评 本题难度不大,主要考查了根据化学方程式来计算有关的量,从而使学生来认识化学反应的本质,代入化学方程式计算的数据必须是纯净物的质量才行.

练习册系列答案
相关题目
6.推理是化学学习中常用的思维方法.下列推理正确的是( )
| A. | 铁在潮湿的空气中容易被锈蚀,所以金属在潮湿的空气中都容易被锈蚀 | |
| B. | 原子在化学变化中不能再分,则分子在化学变化中也不能再分 | |
| C. | 某化肥中加入碱液,无氨味产生,所以该化肥一定不是氮肥 | |
| D. | 化合物是由不同种元素组成的,所以不同种元素组成的纯净物一定是化合物 |
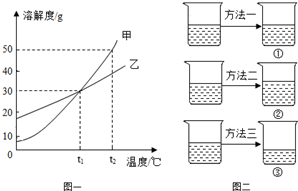
3. 如是a、b、c三种物质的溶解度曲线.下列分析不正确的是( )
如是a、b、c三种物质的溶解度曲线.下列分析不正确的是( )
 如是a、b、c三种物质的溶解度曲线.下列分析不正确的是( )
如是a、b、c三种物质的溶解度曲线.下列分析不正确的是( )| A. | 要配制相同质量分数的a、c两种物质的饱和溶液,应该将温度控制在t1℃ | |
| B. | 将t2℃时a、b、c三种饱和溶液分别降温至t1℃,所得溶液的溶质质量分数最大的是b溶液 | |
| C. | 将c物质的饱和溶液转化为不饱和溶液可以采用加水或降温的方法 | |
| D. | t2℃时,将30ɡ a物质加入50ɡ水中不断搅拌,形成的溶液中溶质质量分数是37.5% |
20.某粒子X2-核外有18个电子,核内有16个中子,下列有关该粒子的说法中,正确的是( )
| A. | 属于金属元素 | B. | 性质稳定 | ||
| C. | 易得到两个电子 | D. | 相对原子质量为32g |
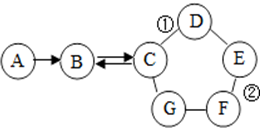 如图所示的是物质A~G相互间的关系(“->”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应).A、F都是单质;F是使用最多的金属材料;B是导致温室效应的主要气体;C在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产等;D可用来改良酸性土壤;E是一种蓝色的硫酸盐溶液.请回答:
如图所示的是物质A~G相互间的关系(“->”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应).A、F都是单质;F是使用最多的金属材料;B是导致温室效应的主要气体;C在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产等;D可用来改良酸性土壤;E是一种蓝色的硫酸盐溶液.请回答: