题目内容
1.善于观察是学习化学的重要方法之一,下列有关实验现象描述正确的是( )| A. | 将氧化铜粉末加入到氢氧化钠溶液中,有蓝色絮状沉淀生成 | |
| B. | 打开浓盐酸瓶盖,瓶口冒白雾 | |
| C. | 铁丝在空气中燃烧,剧烈燃烧,火星四射,生成一种黑色固体 | |
| D. | 硫在空气中燃烧,发出淡蓝色火焰,生成二氧化硫气体 |
分析 A、根据碱的性质分析;
B、根据浓盐酸具有挥发性,进行分析判断.
C、铁丝在空气中不能燃烧;
D、根据硫燃烧的现象分析.
解答 解:A、氧化铜粉不会与氢氧化钠溶液反应,不会有蓝色絮状沉淀生成,故A错误;
B、浓盐酸具有挥发性,打开盛浓盐酸的瓶塞,有白雾生成,而不是白烟,故正确;
C、铁丝在空气中不能燃烧,故错误;
D、硫在空气中燃烧,生成二氧化硫气体是结论,而不是现象,故错误;
故选:B.
点评 本题难度不大,掌握浓盐酸具有挥发性、碱的化学性质、常见物质燃烧的现象等即可正确解答,在描述实验现象时,需要注意烟和雾、实验结论和实验现象的区别

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
11.有三瓶标签模糊不清的无色溶液:稀盐酸、澄清石灰水和氯化钠溶液,下列试剂或用品不能将上述三种溶液一次鉴别出来的是( )
| A. | MgCl2溶液 | B. | Na2CO3溶液 | C. | PH试纸 | D. | 石蕊试液 |
12.铁暴露在空气中会生锈.不知你注意了没有,将苹果切开不久,果肉上就会产生一层咖啡色的物质,也好象是生了“锈”一样.某化学活动小组对此进行了探究.
【提出问题】切开的苹果“生锈”与什么因素有关?
猜想与假设】
猜想①:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”.
猜想②:可能是果肉中的物质与空气中的氧气作用而“生锈”.
猜想③:可能是果肉中的物质与空气中的氮气作用而“生锈”.
猜想④:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”.
猜想⑤:可能是果肉中的物质与空气中的氧气作用而“生锈”,并且苹果“生锈”的速度还可能与温度有关.
【收集证据】
(一)查阅有关资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的二种物质发生反应,生成咖啡色的物质.
(二)实验探究:针对上面的猜想①至猜想⑤,化学活动小组依次设计了实验方案,进行了实验验证,并依次观察到下列实验现象.请你将他们设计的可行的实验探究方案,填写在下表中.
【得出结论】果肉中的与空气中的氧气作用而“生锈”,并且温度越高,苹果“生锈”的速度越快.
【反思与评价】
(1)在②~⑤四种猜想中,你认为猜想③(填代号)最不合理,理由是常温下氮气的化学作用很稳定.
(2)在验证猜想①时,同学们发现,如果水不与空气隔绝,果肉放在水中时间长了也会变色,其可能的原因是溶解在水中的氧气和果肉中的物质发生了反应.
【应用】根据上述结论,要防止果汁变质,果品加工厂加工和保存果汁时可采取的措施是保持低温、隔绝氧气.
【提出问题】切开的苹果“生锈”与什么因素有关?
猜想与假设】
猜想①:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”.
猜想②:可能是果肉中的物质与空气中的氧气作用而“生锈”.
猜想③:可能是果肉中的物质与空气中的氮气作用而“生锈”.
猜想④:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”.
猜想⑤:可能是果肉中的物质与空气中的氧气作用而“生锈”,并且苹果“生锈”的速度还可能与温度有关.
【收集证据】
(一)查阅有关资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的二种物质发生反应,生成咖啡色的物质.
(二)实验探究:针对上面的猜想①至猜想⑤,化学活动小组依次设计了实验方案,进行了实验验证,并依次观察到下列实验现象.请你将他们设计的可行的实验探究方案,填写在下表中.
| 猜想 | 可行的实验方案 | 可观察到的实验现象 |
| 猜想1 | 将一小块果肉浸入盛有蒸馏水的烧杯中 | 果肉表面不变色 |
| 猜想2 | 果肉表面变色 | |
| 猜想3 | 将一小块果肉放入一瓶装有氧气气体的瓶中 | 果肉表面不变色 |
| 猜想4 | 果肉表面不变色 | |
| 猜想5 | 温度高的先变色 |
【反思与评价】
(1)在②~⑤四种猜想中,你认为猜想③(填代号)最不合理,理由是常温下氮气的化学作用很稳定.
(2)在验证猜想①时,同学们发现,如果水不与空气隔绝,果肉放在水中时间长了也会变色,其可能的原因是溶解在水中的氧气和果肉中的物质发生了反应.
【应用】根据上述结论,要防止果汁变质,果品加工厂加工和保存果汁时可采取的措施是保持低温、隔绝氧气.
16.已知空气中完全燃烧1.6g某纯净物生成4.4gCO2和3.6H2O,则该纯净物的组成中( )
| A. | 只有C元素 | B. | 一定含有C、H元素,可能含O元素 | ||
| C. | 一定含有C、H、O元素 | D. | 都不正确 |
13.下列叙述中属于化学性质的描述的是( )
| A. | 通常氧气是无色无味的气体 | |
| B. | 硫在氧气中燃烧,生成无色有刺激性气味的有毒气体 | |
| C. | 在点燃的条件下,细铁丝能在氧气中能燃烧 | |
| D. | 加压、降温时,氧气由气态变成淡蓝色的液态氧 |
10.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图.下列说法正确的是( )
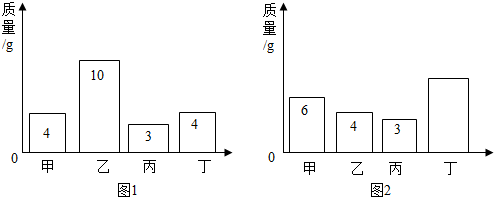

| A. | 该反应为化合反应 | B. | 参加反应的乙、丁质量比为3:2 | ||
| C. | 丙是该反应的催化剂 | D. | 丁相对分子质量是甲的2倍 |
