题目内容
8.二氧化硫是一种有刺激性气味的气体,其水溶液叫亚硫酸(H2SO3);硫化氢(H2S)是一种具有臭鸡蛋气味的气体,其水溶液叫氢硫酸(H2S);又知相同条件下氢硫酸的酸性小于亚硫酸.室温下向饱和H2SO3溶液通入过量H2S气体,反应的化学方程式为:2H2S+H2SO3═3S↓+3H2O.从以上信息得出的下列结论中,不正确的是( )| A. | 反应后液体仍然为酸性 | |
| B. | “臭鸡蛋气味的气体”描述的是硫化氢的物理性质 | |
| C. | SO2与水反应生成亚硫酸,说明SO2与CO2有相似的化学性质 | |
| D. | 在上述过程中,溶液的质量和离子数量一直减小 |
分析 根据题中信息结合溶液的酸碱性、物质的物理性质以及硫化氢气体溶于水进行分析.
解答 解:A、氢硫酸显酸性,又“通入过量H2S气体”,所以反应后液体仍然为酸性,故说法正确;
B、“臭鸡蛋气味的气体”是不需要发生化学变化就能表现出来的性质,描述的是硫化氢的物理性质,故说法正确;
C、二氧化碳与水反应生成碳酸,SO2与水反应生成亚硫酸,说明SO2与CO2有相似的化学性质,故说法正确;
D、硫化氢气体溶于水,形成氢硫酸,所以H2S与H2SO3的反应中溶液的质量和离子数量在减少,而反应完毕后,溶液的质量和离子在增加,故说法错误.
故选:D.
点评 本题难度不大,掌握物理性质的概念等并结合题中信息进行分析即可正确解答本题.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
18.X、Y、Z三种物质,它们之间的转化关系为:X$\stackrel{加盐酸}{→}$Y$\stackrel{Na_{2}CO_{3}}{→}$Z$\stackrel{高温}{→}$X,则X是( )
| A. | Mg | B. | K2O | C. | CaO | D. | Ca(OH)2 |
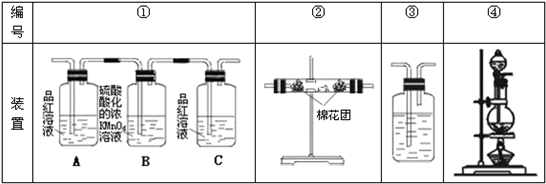
19.根据如图所示实验装置,回答下列问题:
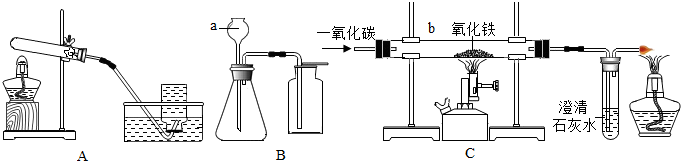
(1)仪器a的名称是长颈漏斗;
(2)几种常见气体的溶解性和密度如表:
实验室可以用装置A完成的实验是①(填序号);
①加热高锰酸钾制取氧气 ②金属锌与稀盐酸反应制取氢气 ③大理石与稀盐酸反应制取二氧化碳 ④加热氯化铵与氢氧化钙固体制取氨气
(3)装置C中硬质玻璃管b内可以观察到的现象为红色粉末变黑,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.

(1)仪器a的名称是长颈漏斗;
(2)几种常见气体的溶解性和密度如表:
| 气体 | 氧气 | 氢气 | 二氧化碳 | 氨气 |
| 溶解性 | 不易溶于水 | 难溶于水 | 能溶于水 | 易溶于水 |
| 密度 | 略大于空气 | 小于空气 | 大于空气 | 小于空气 |
①加热高锰酸钾制取氧气 ②金属锌与稀盐酸反应制取氢气 ③大理石与稀盐酸反应制取二氧化碳 ④加热氯化铵与氢氧化钙固体制取氨气
(3)装置C中硬质玻璃管b内可以观察到的现象为红色粉末变黑,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
20.下列物质不能由金属和酸反应直接制得的是( )
| A. | ZnCl2 | B. | FeCl3 | C. | MgCl2 | D. | AlCl3 |
17.地沟油,城市下水道里悄悄流淌的垃圾,比真正的食用油多了许多致病、致癌的毒性物质.地沟油主要成分是甘油三酯(C39H74O6),下列有关甘油三酯的说法不正确的是( )
| A. | 该物质由三种元素组成 | |
| B. | 甘油三酯中碳元素、氢元素、氧元素的质量比是39:74:6 | |
| C. | 每个甘油三酯分子由119个原子构成 | |
| D. | 甘油三脂是一种有机物 |
3.如图为氮元素在元素周期表中的信息及原子结构示意图.下列有关说法不正确的是( )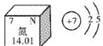

| A. | 氮元素属于非金属元素 | B. | 氮原子核外有2个电子层 | ||
| C. | 氮元素内质子数为7 | D. | 氮元素的相对原子质量是14.01g |