题目内容
1.下列基本实验操作正确的是( )| A. |  氢气验纯 | B. |  闻气体气味 | C. |  检查气密性 | D. |  取固体药品 |
分析 根据已有的实验操作结合图示进行分析解答即可.
解答 解:A、检验氢气的纯度的实验操作是正确的;
B、闻气体气味时不能将鼻孔凑到容器口,错误;
C、该装置中有长颈漏斗,不能使用该方法检查装置的气密性,错误;
D、取固体药品时,瓶塞要倒放,错误;
故选A.
点评 本题考查的是常见的实验操作,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
12.高铁酸钾(K2FeO4)是一种新型高效水处理剂.下列关于该物质的叙述,正确的是( )
| A. | 它是一种氧化物 | |
| B. | 组成中含有地壳中含量最多的金属元素 | |
| C. | 它是一种化合物 | |
| D. | K2FeO4中铁元素的化合价为+3 |
13.下列溶液中,能使酚酞变红色的是( )
| A. | 烧碱溶液 | B. | 稀硫酸 | C. | 稀盐酸 | D. | 氯化钠溶液 |
10.碳酸钠用途非常广泛,是工业生产中重要的化工原料.在1921年我国科学家侯德榜创造了一种著名的纯碱生产方法--“联合制碱法”.“联合制碱法”生产过程:
(1)第一步主要反应为NH3+CO2+H2O═NH4HCO3 该反应属于化合反应基本反应类型.
(2)第二步用食盐与NH4HCO3反应.食盐来源于某盐田,该粗盐主要含有氯化钠,此外还含有少量硫酸钠,氯化钙和氯化镁.经净化、精制得到生产碳酸钠所需要的食盐水,其主要流程如图1:
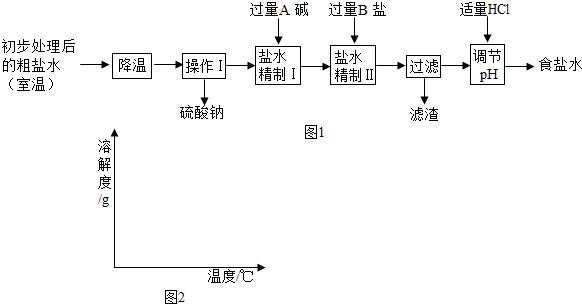
①通过降温使硫酸钠从粗盐水中析出,其原理是氯化钠和硫酸钠的溶解度与温度的变化差异较大,请在溶解度图(如图2)中简单画出氯化钠和硫酸钠的溶解度曲线变化趋势图.
②“精制I”操作中,加入过量含钙元素的碱的化学式是Ca(OH)2.
其反应化学方程示为Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2.
③“精制II”操作中,加入B盐的有关反应方程式为CaCl2+Na2CO3=2NaCl+CaCO3↓;Ca(OH)2+Na2CO3=2NaOH+CaCO3↓.
④为保证“精制II”操作中过量B盐把杂质全部除去,请在下表中写出检验溶液中B盐是否过量的实验报告.
⑤查阅资料得知NaCl、NH4HCO3、NaHCO3、NH4Cl在30℃时的溶解度如下表所示:
请根据溶解度表所提供的信息,写出“联合制碱法”中的第二步属于复分解反应的化学方程式:NH4HCO3+NaCl=NaHCO3↓+NH4Cl.
(3)第三步处理制得碳酸钠,反应原理为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+H2O+CO2↑
(1)第一步主要反应为NH3+CO2+H2O═NH4HCO3 该反应属于化合反应基本反应类型.
(2)第二步用食盐与NH4HCO3反应.食盐来源于某盐田,该粗盐主要含有氯化钠,此外还含有少量硫酸钠,氯化钙和氯化镁.经净化、精制得到生产碳酸钠所需要的食盐水,其主要流程如图1:

①通过降温使硫酸钠从粗盐水中析出,其原理是氯化钠和硫酸钠的溶解度与温度的变化差异较大,请在溶解度图(如图2)中简单画出氯化钠和硫酸钠的溶解度曲线变化趋势图.
②“精制I”操作中,加入过量含钙元素的碱的化学式是Ca(OH)2.
其反应化学方程示为Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2.
③“精制II”操作中,加入B盐的有关反应方程式为CaCl2+Na2CO3=2NaCl+CaCO3↓;Ca(OH)2+Na2CO3=2NaOH+CaCO3↓.
④为保证“精制II”操作中过量B盐把杂质全部除去,请在下表中写出检验溶液中B盐是否过量的实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| 温度 | NH4Cl | NH4HCO3 | NaHCO3 | NaCl |
| 30℃ | 41.1g | 27.0g | 11.1g | 36.3g |
(3)第三步处理制得碳酸钠,反应原理为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+H2O+CO2↑
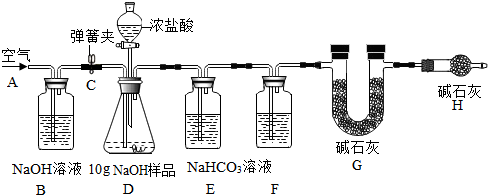
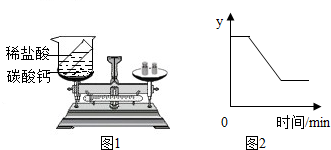 根据质量守恒定律,回答下列问题.Ⅰ、为验证质量守恒定律,某同学设计了如图的实验.
根据质量守恒定律,回答下列问题.Ⅰ、为验证质量守恒定律,某同学设计了如图的实验.