题目内容
实验室有一瓶标签被腐蚀的盐酸,小丽为了测定溶液中溶质的质量分数,在烧杯中
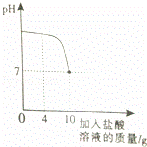
配制了8g 10%的NaOH溶液.然后往烧杯中滴加该盐酸.反应过程中溶液的pH与滴入盐酸的质量关系如图所示.请回答下列问题:
(1)配制了8g 10%的NaOH溶液,需要水的质量为 ;
(2)计算该盐酸的溶质质量分数;(写出计算过程)
(3)当滴入4g盐酸时,烧杯内溶液中钠元素的质量为 g.
| 根据化学反应方程式的计算;有关溶质质量分数的简单计算. | |
| 专题: | 综合计算(图像型、表格型、情景型计算题). |
| 分析: | 根据氢氧化钠溶液的质量及其氢氧化钠的质量分数可以计算水的质量; 根据加入盐酸的质量可以计算该盐酸的溶质质量分数; 无论滴加盐酸的质量为多少,溶液中钠元素的质量等于氢氧化钠溶液中钠元素的质量. |
| 解答: | 解:(1)配制8g10%的NaOH溶液,需要水的质量为:8g×(1﹣10%)=7.2g; 故填:7.2g. (2)设10g稀盐酸中氯化氢的质量为x, NaOH+HCl═NaCl+H2O, 40 36.5 8g×10% x
x=0.73g, 该盐酸的溶质质量分数为: 答:该盐酸的溶质质量分数为7.3%. (3)当滴入4g盐酸时,烧杯内溶液中钠元素的质量为:8g×10%× 故填:0.46. |
| 点评: | 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性. |

下列有关资源、能源的说法错误的是( )
|
| A. | 我国金属资源储量丰富,可以任意开采 |
|
| B. | 太阳能、风能、核能、氢能都属于新能源 |
|
| C. | 空气是一种宝贵资源,其中含量最多的是N2 |
|
| D. | 石油经加热炼制,可得到汽油、煤油、柴油等不同产品 |
下列图象能正确反映对应的变化关系的是( )
|
| A. | 盐酸中加水 |
|
| B. |
将生锈严重的铁钉加入到足量的稀盐酸中 |
|
| C. |
用等质量、等质量分数的H2O2溶液来制取O2 |
|
| D. |
将过量的等质量的镁和锌跟别加入到等质量、等质量分数的稀盐酸中 |
下列探究燃烧条件的实验中,只能得出燃烧需要氧气结论的是( )
|
| A. |
| B. |
| C. |
| D. |
|
下列各组物质在溶液中能大量共存且形成无色溶液的是( )
|
| A. | NaOH NHO3 NH4NO3 | B. | KNO3 CaCl2 HCl |
|
| C. | H2SO4 FeCl3 NaNO3 | D. | NaCl BaCl2 Na2CO3 |
下列说法中正确的是( )
|
| A. | 废旧电池可以随意丢弃 | B. | 铁矿石可以随意开采 |
|
| C. | 被腐蚀的铁制品应该加以回收利用 | D. | 铁丝在氧气中燃烧生成氧化铁 |
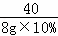 =
=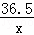 ,
,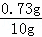 ×100%=7.3%,
×100%=7.3%,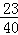 ×100%=0.46g,
×100%=0.46g,


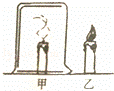




 ,图中与其化学性质相似的元素是 ;
,图中与其化学性质相似的元素是 ; 在一次用餐中,同学们对燃料“固体酒精”产生了好奇,遇事对其成分进行研究。
在一次用餐中,同学们对燃料“固体酒精”产生了好奇,遇事对其成分进行研究。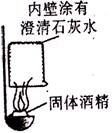 【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成。(2)氯化钙、氯化钡溶液均呈中性。
【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成。(2)氯化钙、氯化钡溶液均呈中性。 ,有气泡产生。写出产生气体的化学方程式_________________________________。
,有气泡产生。写出产生气体的化学方程式_________________________________。 甲组取烧杯上层清夜于两支试管中,按下图探究。
甲组取烧杯上层清夜于两支试管中,按下图探究。
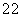 乙组认为甲组实验不能证明清夜中一定有氢氧化钠,理由是____________
乙组认为甲组实验不能证明清夜中一定有氢氧化钠,理由是____________