题目内容
4.请你根据对金属和金属材料的认识,回答下列问题.
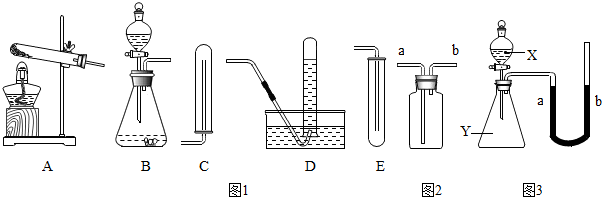
(1)如图1标出的是组成灯泡的物质,所标出的物质中不属于金属材料的是氮气、玻璃.
(2)钢铁厂以赤铁矿为原料冶炼生铁的原理为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(用化学方程式表示).很多大型场馆的建设使用了大量的钢材,主要是因为钢比纯铁具有硬度大的优良性能.
(3)工人师傅切割铁板时,用硫酸铜溶液在铁板上划线可以留下红色痕迹,该变化的原理是Fe+CuSO4=FeSO4+Cu(用化学方程式表示).将生铁加入足量的稀盐酸中,充分反应后得到浅绿色溶液,该洛液中含有的金属离子主要是Fe2+(写符号),溶液底部残留的黑色不溶物主要是碳•
(3)某化学兴趣小组的同学在探究锌、铜、铁三种金属的有关性质时,进行了如图2所示实验:
①在A实验中发生反应的化学方程式为Fe+CuSO4=FeSO4+Cu.
②将A实验结束后①、②试管内的物质倒入烧杯中,发现烧杯中的红色固体物质明显增多,一段时间后过滤,同学们向滤渣中滴加稀盐酸,结果没有气泡产生,那么滤液中一定含有的溶质是硫酸锌和硫酸亚铁.
分析 根据已有的物质的材料类别进行分析解答,一氧化碳能与氧化铁高温反应生成铁和二氧化碳;铁能与硫酸铜反应生成硫酸亚铁和铜,根据已有的金属活动性顺序的意义进行分析解答即可.
解答 解:(1)氮气和玻璃不是金属材料,故填:氮气、玻璃;
(2)一氧化碳能与氧化铁高温反应生成铁和二氧化碳,钢材的硬度比纯铁大,故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,硬度大;
(3)用硫酸铜溶液在铁板上划线可以留下红色痕迹,是因为铁能与硫酸铜反应生成硫酸亚铁和铜,生铁的成分是铁和碳,铁能与盐酸反应生成氯化亚铁和氢气,碳不反应,故剩余的黑色固体是碳,故填:Fe+CuSO4=FeSO4+Cu,Fe2+,碳;
(4)①铁能与硫酸铜反应生成硫酸亚铁和铜,故填:Fe+CuSO4=FeSO4+Cu;
②向滤渣中滴加稀盐酸,结果没有气泡产生,说明滤渣中不含有铁,因此滤液中一定含有硫酸锌和生成的硫酸亚铁,故填:硫酸锌和硫酸亚铁.
点评 掌握常见的金属的性质以及金属活动性顺序的意义是正确解答本题的关键.

练习册系列答案
相关题目
12.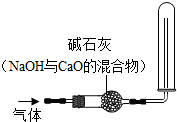 以下几种气体,不能用图装置干燥并收集的是( )
以下几种气体,不能用图装置干燥并收集的是( )
①H2 ②O2 ③CO2 ④SO2 ⑤CH4⑥HCl.
 以下几种气体,不能用图装置干燥并收集的是( )
以下几种气体,不能用图装置干燥并收集的是( )①H2 ②O2 ③CO2 ④SO2 ⑤CH4⑥HCl.
| A. | ①② | B. | ①⑤ | C. | ①②⑤ | D. | ②③④⑥ |
19.下列食物的近似pH如下,其中碱性最强的是( )
| A. | 鸡蛋清7.6~8.0 | B. | 柠檬2.2~2.4 | C. | 西红柿4.0~4.4 | D. | 牛奶6.3~6.6 |
9.下列物质的分类正确的是( )
| A. | 空气是化合物 | B. | 水是氧化物 | C. | 液氧是混合物 | D. | 碘酒是纯净物 |