题目内容
19.下列说法正确的是( )| A. | K2MnO4、KMnO4、MnO2三者中Mn元素的化合价逐渐升高 | |
| B. | HCl、NaCl、Na2CO3溶液的pH逐渐变大 | |
| C. | NH4NO3、NaCl、CaO三者溶于水后,所得溶液的温度逐渐降低 | |
| D. | 将Zn、Fe两金属片分别放入CuSO4溶液中可以证明三种金属的活动性顺序为Zn>Fe>Cu |
分析 A、根据在化合物中正负化合价代数和为零进行分析解答;
B、根据已有的知识进行分析解答,酸性溶液的pH小于7,碱性溶液的pH大于7,中性溶液的pH等于7,据此解答;
C、根据物质溶于水溶液的温度变化情况分析;
D、前边的金属会把后边的金属从其盐溶液中置换出来.
解答 解:A、根据在化合物中正负化合价代数和为零,氧显-2价,钾显+1价,氯显-1价,K2MnO4中Mn元素的化合价为+6价;KMnO4中Mn元素的化合价为+7价;MnO2中Mn元素的化合价为+4价;故错误;
B、盐酸呈酸性,pH小于7,氯化钠溶液呈中性,pH等于7,碳酸钠溶液呈碱性,pH大于7,故正确;
C、NH4NO3、NaCl、CaO三者溶于水后,所得溶液的温度变化分别是降低、不变、升高,故错误;
D、根据Zn、Fe两金属能置换CuSO4溶液中铜,只能说明Zn、Fe两金属活动性比Cu强,但不能判断Zn、Fe两金属活动性强弱关系,不能确定Zn、Fe、Cu三种金属的活动性顺序.故错误;
故选:B.
点评 本题难度不大,掌握元素化合价的计算方法、溶液的酸碱性、物质溶于水后温度变化情况以及金属的活动性强弱等是解决此题的关键.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
9.化学就在我们身边,它与我们的生活息息相关.
(1)上表为某食品包装袋上的部分说明.请回答下列问题:
①在饼干的配料中,属于油脂的是植物油;
②配料中可用于腌渍蔬菜的物质是食盐;
③小麦粉中富含糖类,糖类在人体内经过一系列的变化最终转化为水和CO2(或二氧化碳);
④食用香精中含有香豆素(C9H6O2),香豆素中碳、氢、氧三种元素的质量比为54:3:16.
(2)下列电动自行车的各组件中,属于有机合成材料的是c;
a.铜线电机 b.钢质车轮 c.塑料灯罩
(3)啤酒酿造需要大量的软水,生活中常用肥皂水区别软水和硬水.
| 商品名称 | ××饼干 |
| 配料 | 小麦粉、植物油、鲜鸡蛋、食盐、膨松剂、食用香精等 |
| 规格 | 400g |
| 储藏方法 | 存放于阴凉干燥处,避免阳光直射 |
| 保质期 | 270天 |
①在饼干的配料中,属于油脂的是植物油;
②配料中可用于腌渍蔬菜的物质是食盐;
③小麦粉中富含糖类,糖类在人体内经过一系列的变化最终转化为水和CO2(或二氧化碳);
④食用香精中含有香豆素(C9H6O2),香豆素中碳、氢、氧三种元素的质量比为54:3:16.
(2)下列电动自行车的各组件中,属于有机合成材料的是c;
a.铜线电机 b.钢质车轮 c.塑料灯罩
(3)啤酒酿造需要大量的软水,生活中常用肥皂水区别软水和硬水.
11.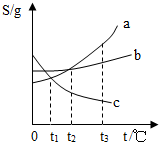 现有溶解度曲线如图,下列有关说法正确的是( )
现有溶解度曲线如图,下列有关说法正确的是( )
 现有溶解度曲线如图,下列有关说法正确的是( )
现有溶解度曲线如图,下列有关说法正确的是( )| A. | t2℃时a、b两物质溶液的溶质质量分数相等 | |
| B. | 将c的不饱和溶液降温可以转化为饱和溶液 | |
| C. | 将t3℃时a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液的溶质质量分数大小顺序为b>a>c | |
| D. | 将t3℃的a、b、c 三种物质的饱和溶液冷却到t1 时,a物质析出最多,无c物质析出 |
9.下列变化不能通过一步化学反应实现的是( )
| A. | Cu→Cu(OH)2 | B. | S→SO2 | C. | Fe2O3→Fe2(SO4)3 | D. | CaCO3→CaO |