题目内容
8.在宏观、微观、符号之间建立联系,是化学学科特有的思维方式.(1)在C60、金刚石、硫酸铜三种物质中,由分子构成的物质是C60.
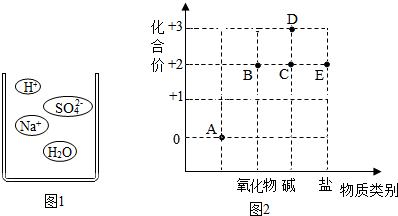
(2)通过分析组成和结构,可以预测物质的某些性质.根据图1硫酸氢钠溶液的微观图示,分析推测NaHSO4的性质,其中合理的是BCD.
A.其水溶液能与金属铁发生置换反应,得到金属钠
B.其水溶液能使紫色石蕊试液变红
C.其水溶液能与金属锌反应生成氢气
D.其水溶液与硝酸钡溶液反应生成硫酸钡沉淀
(3)从微观角度解释下列问题:
①一氧化碳和二氧化碳化学性质不同的原因是分子的构成不同;
②金刚石和石墨物理性质差异很大的原因是碳原子排列方式不同.
(4)以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.图2为铁的价类图,请分析该图后填写:
①A点表示的物质类别是单质.B点表示化合物的化学式为FeO.
②某化合物化学式为(NH4)2Fe(SO4)2,它代表的点是E.(填“A、B、C、D、E”)
③写出由C点表示化合物与氧气、水发生化合反应生成D的化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3.
分析 (1)根据金属、大多数固态非金属单质等由原子构成解答;
(2)根据物质的性质的结构进行分析;
(3)
①根据一氧化碳和二氧化碳化学性质不同,是因为它们分子的构成不同解答;
②根据金刚石和石墨物理性质差异很大,是原因是碳原子排列方式不同解答;
(4)①根据单质化合价为零和氧化铁的颜色考虑;②根据在化合物中正负化合价代数和为零计算出铁的化合价;③根据方程式的写法写出化学方程式.
解答 解:
(1)硫酸铜是由铜离子和硫酸根离子构成的;C60是由C60分子构成的;金刚石属于固态非金属单质,是由碳原子直接构成的;
(2)
A.其水溶液不能与金属钾发生置换反应,错误;
B.其水溶液呈酸性,能使紫色石蕊试液变红,正确;
C.其水溶液呈酸性,能与金属锌反应生成氢气,正确;
D.其水溶液中含有硫酸根离子,与硝酸钡溶液反应生成硫酸钡沉淀,正确.
(3)
①一氧化碳和二氧化碳化学性质不同,是因为它们分子的构成不同,不同种的分子性质不同.
②金刚石和石墨物理性质差异很大,是原因是碳原子排列方式不同.
(4)①单质化合价为零,由图示可知A点物质的化合价是零,所以物质类别是单质;B点是铁的氧化物,铁的化合价是+2,所以物质是氧化亚铁;
②铵根的化合价是+1价,硫酸根的化合价是-2价,设铁元素化合价是x则:(+1)×2+x+(-2)×2=0,解得x=+2,该物质属于盐,所以是E点;
③反应物是氢氧化亚铁、氧气和水,生成物是氢氧化铁,用观察法配平,所以方程式是:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
答案:
(1)C60
(2)BCD;
(3)①分子的构成不同; ②碳原子排列方式不同;
(4)①单质; FeO; ②E; ③4Fe(OH)2+O2+2H2O=4Fe(OH)3
点评 本题难度不大,掌握分子的基本性质(可以简记为:“两小运间,同同不不”)及利用分子的基本性质分析和解决问题的方法是解答此类题的关键.

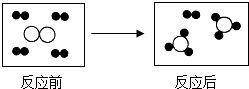
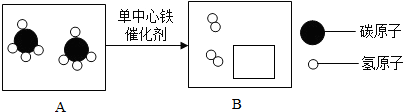
| A. | 反应后生成两种物质 | |
| B. | 参加反应各物质的分子个数比为1:4 | |
| C. | 反应前后原子的种类没有改变 | |
| D. | 该反应的基本类型是置换反应 |
| A. |  | B. |  | C. |  | D. |  |
| A. | 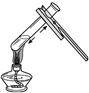 加热液体 | B. | 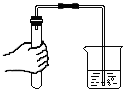 检查装置气密性 检查装置气密性 | C. | 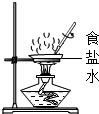 蒸发食盐水 | D. | 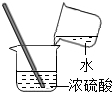 稀释浓硫酸 |
| 温度/℃ | 10 | 20 | 30 | 40 | |
| 溶解度 g/100gH2O | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 | |
②碳酸钠溶液中混有少量的氯化钠,可通过降温结晶(或冷却热的饱和溶液)的方法提纯;
③碳酸钠的溶解度随温度的升高而增大(填“增大”或“减小”).在20℃时,将100g水加入30g碳酸钠中,充分搅拌后得到的是饱和(填“饱和”或“不饱和”)溶液,将上述溶液升温到30℃,该溶液的溶质质量分数为23.1%.