题目内容
3.小刚同学在学习了酶的知识后了解到了酶的催化作用要受到温度、酸碱度(pH)的影响.联系到前面学习的知识,小刚同学又提出了自己的一个猜想:酶的催化作用可能会受到重金属离子的影响.结合猜想小刚进行了如下探究:【查阅资料】重金属指密度大于5克/厘米3的金属(一般指密度大于4.5克/厘米3的金属).
【设计实验】取试管4支,编号,按表分别加入试剂,摇匀,迅速置于37℃的水浴中,10分钟后取出,冷却后分别加入碘液3滴,观察其颜色变化.
| 编号 | 0.25%淀粉溶液(ml) | 蒸馏水(ml) | 0.3%NaCl溶液(ml) | 1%CuSO4溶液(ml) | 唾液溶液(ml) | 加入碘液3滴后现象 |
| 1 | 3 | 2 | - | - | - | 变蓝色 |
| 2 | 3 | 1 | - | - | 1 | 不变蓝 |
| 3 | 3 | - | 1 | - | 1 | 不变蓝 |
| 4 | 3 | - | - | 1 | 1 | 变蓝色 |
根据小刚同学的探究过程回答下列问题:
(1)小刚同学提出猜想的依据是:酶是一种蛋白质,遇到重金属离子会变性,从而丧失活性.
(2)比较上述实验中的1号和2号试管及观察到的现象,你可得出的结论是:唾液淀粉酶能催化淀粉的分解.
(3)在看了小刚的设计及实验后,同桌的小王认为凭上述实验还不足以证明小刚的猜想.小王提出应该将实验中的CuSO4溶液更换成CuCl2溶液才更有说服力.如果你也同小王一起探究,你还可以建议小刚作怎样的更换?将NaCl溶液换成Na2SO4溶液.
(4)在生活中重金属盐类通常也被作为消毒杀菌的药物来使用,如图所示为硝酸银滴眼液的药品说明书的一部分,其中有一条注意事项,你能用所学的科学知识解释:为什么可以用0.9%的生理盐水来减轻硝酸银的腐蚀性?(用化学方程式表示)NaCl+AgNO3=NaNO3+AgCl↓.

(5)随着工业的不断发展,重金属污染越来越严重,重金属中毒事件也越来越常见,因此了解一些必要的急救措施对我们来说很重要.若有人误食被电镀厂废水(含铬(Cr)、镍(Ni)、镉(Cd))污染的食物而急性中毒,为解毒,下列四种供选物质中你不应该选择的是④.
①鸡蛋清 ②鲜豆浆 ③鲜牛奶 ④糖水.
分析 (1)酶具有1、高效性 2、专一性 3、多样性 4、温和性 5、活性可调节性 6.有些酶的催化性与辅因子有关 7.易变性 大多数酶是蛋白质,因而会被高温、酸、强碱等破坏;
(2)通过观察图可知,不同的是1号试管加入的是水,2号试管加入的是唾液,该实验设置了对照实验,变量是唾液,目的是探究唾液对淀粉的消化作用;
(3)根据控制变量分析;
(4)氯化钠可以将银离子转化为沉淀,
(5)根据重金属盐中毒的原理判断,即破坏人体的蛋白质结构,使之失去生理功能;重金属可使蛋白质变性而中毒,误食重金属盐,可马上服用大量的豆浆或牛奶,可起到缓冲的作用.
解答 解:(1)小刚同学提出猜想的依据是:酶是一种 蛋白质,遇到重金属离子会变性,从而丧失活性.
(2)1号试管加入的是水,滴加碘液变蓝,2号试管加入的是唾液,滴加碘液不变蓝,比较上述实验中的1号和2号试管及观察到的现象,你可得出的结论是:唾液淀粉酶能分解淀粉.
(3)实验中盐用的是NaCl溶液和CuSO4溶液,除了金属离子不同,酸根离子也不同,可以将将实验中的CuSO4溶液更换成CuCl2溶液或将NaCl溶液换成Na2SO4溶液;
(4)氯化钠可以硝酸银反应,将银离子转化为沉淀,方程式为:NaCl+AgNO3=NaNO3+AgCl↓
(5)重金属盐中毒的原理即破坏人体的蛋白质结构,蛋清的主要成分是蛋白质.鸡蛋清、豆浆、牛奶中含有蛋白质,服用鸡蛋清、豆浆、牛奶,可防止人体本身的蛋白质被破坏,能用于解毒,而糖水不能用于解毒.
故答案为:(1)蛋白质;
(2)唾液淀粉酶能催化淀粉的分解;
(3)将NaCl溶液换成Na2SO4溶液;
(4)NaCl+AgNO3=Na NO3+AgCl↓;
(5)④.
点评 本题考查蛋白质的性质,题目难度不大,了解中毒原理、或事故发生原因,才会正确对事故进行处理,保障人的生命安全.

 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案探究一:检验红色固体产物的成份
【查阅资料】Ⅰ.木炭还原氧化铜除生成铜外还可能生成氧化亚铜(Cu2O);
Ⅱ.Cu和Cu2O均为不溶于水的红色固体;Ⅲ.Cu2O+H2SO4═CuSO4+Cu+H2O
【提出问题】该实验的红色固体产物中含有什么物质?
【猜想与假设】假设1:红色固体只含Cu; 假设2:红色固体只含Cu2O;
假设3:红色固体Cu、Cu2O的混合物(请补充完成假设3).
【实验探究】(填写表中空格)
| 实验操作 | 实验现象 | 实验结论 |
| 取少量红色固体加入到足量稀硫酸溶液中 | 若无明显现象 | 假设1成立 |
| 若固体部分(选填“全部”或“部分”)溶解,溶液由无色变蓝色 | 假设2和假设3均成立 |
该化学兴趣小组经交流讨论后,设计了如下两方案:
方案一:称取5.00g红色固体加入到足量稀硫酸溶液中使其充分反应后,操作A、洗涤、干燥,称量得红色固体质量为4.10g.
(1)操作A的名称是过滤,在实验室中完成操作A的玻璃仪器有玻璃棒、烧杯和漏斗;
(2)检验反应后剩余红色固体是否洗涤干净的方法是:取少量最后一次洗涤液,加入氢氧化钠溶液,如果观察到现象:无蓝色沉淀生成,说明已洗涤干净.
(3)通过计算,假设3成立,红色固体产物中Cu2O的含量为1.44g;
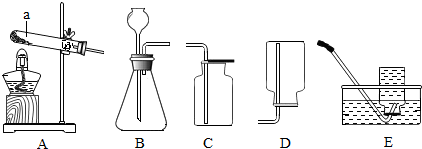
方案二:称取5.00g的红色固体,用如图所示装置进行实验(固定装置略去,碱石灰为氧化钙和氢氧化钠的混合物),通过测定反应前后装置d的质量达到实验目的.
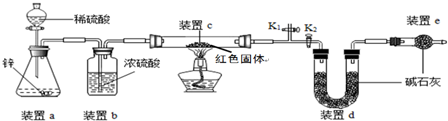
(1)装置a中用稀硫酸而不用稀盐酸,原因是盐酸挥发出氯化氢气体,与d中的物质反应,影响测定结果;
(2)装置b的作用是干燥氢气,若不加装置b,实验结果会偏大(“偏大”或“偏小”);
(3)装置c中涉及的反应化学方程式Cu2O+H2$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+H2O;
(4)装置e的作用是防止空气中CO2及H2O对装置d的测量造成误差,若不加装置e,实验结果会偏大(“偏大”或“偏小”);
(5)点燃酒精灯前涉及的部分操作如下,
①连接仪器;②检查装置的气密性;
③关闭K2,打开K1,通氢气一段时间以赶尽装置内原有的空气,其目的是:a.防止空气中的H2O和CO2进入装置d干扰测定;b.防氢气不纯,发生爆炸,检验空气是否赶尽的方法是:在K1处用小试管收集气体,进行点燃;④打开K2,关闭K1
(6)经测定反应前后装置d的质量分别为100.00g、100.18g,计算产物中Cu2O的含量(写出计算过程,最后结果保留小数点后1位)
【交流与反思】
(1)在方案一实验测定中,若测定结果偏大,则下列可能的原因有①②③.(填序号)
①反应后剩余红色固体未洗涤干净 ②洗涤后未完全干燥
③干燥方法采用的是在空气中加热烘干 ④称量剩余红色固体时,有部分固体洒落到实验台上
(2)方案二中利用同样的装置,还可通过测定反应前后装置c(填“a”、“b”或“c”)的质量达到实验目的.
| A. | 混合物变为纯净物 | B. | 分子间的空隙减小 | ||
| C. | 化学性质发生变化 | D. | 分子总数增加 |
 研究金属与水的反应是研究金属化学性质的重要手段.较高温度下铁粉能与水蒸气反应是铁作为一种较活泼金属的有力证据.某校科学兴趣小组同学利用如图所示装置成功地完成了该实验.在高温下普通铁粉与水蒸气反应,生成铁的氧化物(与铁在氧气中的燃烧产物相同)和氢气,氢气可以在装置右端的支管处被点燃.根据以上信息回答:
研究金属与水的反应是研究金属化学性质的重要手段.较高温度下铁粉能与水蒸气反应是铁作为一种较活泼金属的有力证据.某校科学兴趣小组同学利用如图所示装置成功地完成了该实验.在高温下普通铁粉与水蒸气反应,生成铁的氧化物(与铁在氧气中的燃烧产物相同)和氢气,氢气可以在装置右端的支管处被点燃.根据以上信息回答:(1)铁粉与水蒸气在高温下反应的化学方程式为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;其中还原剂为:铁粉.
(2)同学们对本实验成功的关键因素进行了分析:
①A处湿沙子的作用是提供水蒸汽;
②D处气体通过水的目的是 使氢气中混杂的水蒸汽遇冷液化,使氢气更纯净易于点燃.
(3)同学们还探索了铁粉用量与反应时间的关系,列表如下:(注:反应时间指加热一分钟后收集10毫升气体所需时间)从表中可以看出:铁粉用量与反应时间的关系是反应时间最短,反应速度最快.
| 铁粉质量/g | 0.2 | 0.4 | 0.6 | 0.8 |
| 第一次反应时间/S | 91 | 40 | 45 | 99 |
| 第二次反应时间/S | 84 | 44 | 50 | 82 |
| A. | 混合后溶液的质量分数c%=$\frac{a%+b%}{2}$ | |
| B. | 混合后所得溶液中溶质的溶解度将改变 | |
| C. | 混合后的溶液可能是硝酸钾的饱和溶液 | |
| D. | 混合后所得溶液的质量分数肯定介于a%与b%之间 |
| A. | 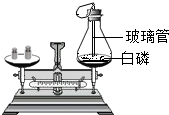 测量白磷燃烧前后质量变化值 | B. | 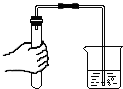 检查装置气密性 | ||
| C. | 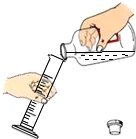 量取液体 | D. |  收集CO2气体 |

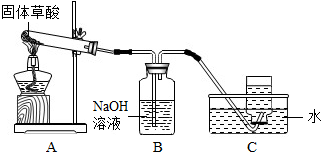 某化学课题小组通过查阅资料得知:固体草酸(H2C2O2•2H2O)受热可分解,其化学方程式(H2C2O2•2H2O═CO↑+CO2↑+3H2O)该课题小组的同学在实验室分别进行了如下实验,请回答下列问题:
某化学课题小组通过查阅资料得知:固体草酸(H2C2O2•2H2O)受热可分解,其化学方程式(H2C2O2•2H2O═CO↑+CO2↑+3H2O)该课题小组的同学在实验室分别进行了如下实验,请回答下列问题: