题目内容
11.通过海水提取的粗盐中含有MgCl2、CaCl2、MgSO4.以及泥沙等杂质.以下是一种制备精盐的实验方案(MgCl2、CaCl2、MgSO4三种试剂均过量).请回答下列问题: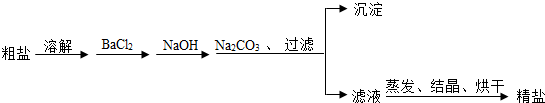
(1)加入Na2CO3的目的是除去CaCl2及过量的BaCl2;
(2)该实验方案还需完善,请写出具体的操作步骤:向滤液中加入适量的稀盐酸,以除去氢氧化钠和碳酸钠.
分析 (1)考虑:氯化钡与MgSO4反应生成氯化镁和硫酸钡沉淀;氯化镁与氢氧化钠反应生成氢氧化镁白色沉淀和氯化钠;氯化钙与碳酸钠反应生成氯化钠和碳酸钙白色沉淀,可以除去氯化钙;
(2)过滤前的溶液中加入的碳酸钠和氢氧化钠都是过量的,反应后两者都有剩余,需要加入一种试剂将溶液中的碳酸根离子和氢氧根离子除去.
解答 解:(1)因为氯化钡与MgSO4反应生成氯化镁和硫酸钡沉淀;氯化镁与氢氧化钠反应生成氢氧化镁白色沉淀和氯化钠;氯化钙与碳酸钠反应生成氯化钠和碳酸钙白色沉淀,可以除去氯化钙,加入Na2CO3的目的是:除去CaCl2及过量的BaCl2;
(2)过滤后滤液的主要成分有:NaCl、NaOH、Na2CO3;要得到纯净的氯化钠,此实验方案尚需完善,具体步骤是:向滤液中加入适量的稀盐酸,以除去氢氧化钠和碳酸钠.
故答案为:
(1)除去CaCl2及过量的BaCl2;
(2)向滤液中加入适量的稀盐酸以除去氢氧化钠和碳酸钠.
点评 除杂质时加入的试剂只能与杂质反应,不能引入新的杂质,将不溶于液体的固体和液体分离用过滤的方法,把可溶性固体与液体分开用蒸发的方法.

练习册系列答案
相关题目
1.不锈钢是在铁中加入铬镍,改变内部结构,从而起到防锈作用.
小明为了探究铬(Cr)、镁、铜的活动性强弱关系,进行如下探究活动:
【提出假设】对三种金属的活动性顺序提出三种可能的假设:
a.Mg>Cr>Cu b.Mg>Cu>Cr c.Cr>Mg>Cu
【设计实验】同温下,取大小相同的打磨过的金属薄片,分别投入到等体积等浓度的足量稀盐酸中,观察现象,记录如表:
【得出结论】原假设中正确的是b(填假设中a、b或c).
【实验讨论】
(1)铬与盐酸反应的化学方程式是Cr+2HCl═CrCl2+H2↑(Cr在生成物中显+2价),该反应的基本反应类型置换反应
(2)小明还想用硫酸铜溶液代替上述实验中的盐酸,在两试管中分别与镁片、铬片混合得出三种金属的活动性关系.小花认为不可行,理由是无法判断铬和镁的活动性顺序.
【拓展迁移】若只有一支盛有少量稀盐酸的试管,只需合理安排金属片的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铬、镁、铜这三种金属的活动性顺序,则三金属片的插入顺序为Cu、Cr、Mg.
小明为了探究铬(Cr)、镁、铜的活动性强弱关系,进行如下探究活动:
【提出假设】对三种金属的活动性顺序提出三种可能的假设:
a.Mg>Cr>Cu b.Mg>Cu>Cr c.Cr>Mg>Cu
【设计实验】同温下,取大小相同的打磨过的金属薄片,分别投入到等体积等浓度的足量稀盐酸中,观察现象,记录如表:
| 金属 | Cr | Mg | Cu |
| 与盐酸反应的现象 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生剧烈,金属迅速溶解 | 无气泡产生,金属无变化 |
【实验讨论】
(1)铬与盐酸反应的化学方程式是Cr+2HCl═CrCl2+H2↑(Cr在生成物中显+2价),该反应的基本反应类型置换反应
(2)小明还想用硫酸铜溶液代替上述实验中的盐酸,在两试管中分别与镁片、铬片混合得出三种金属的活动性关系.小花认为不可行,理由是无法判断铬和镁的活动性顺序.
【拓展迁移】若只有一支盛有少量稀盐酸的试管,只需合理安排金属片的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铬、镁、铜这三种金属的活动性顺序,则三金属片的插入顺序为Cu、Cr、Mg.
2.下列化学用语书写正确的是( )
| A. | 钙离子的符号$\stackrel{+2}{Ca}$ | B. | 硝酸钾的化学式:KNO3 | ||
| C. | 水的化学式:H2O2 | D. | 氧元素的符号:O2 |
16.下列饮品属于溶液的是( )
| A. | 牛奶 | B. | 蔗糖水 | C. | 豆浆 | D. | 果粒橙 |
3. 如图是工业上在一定条件下制取乙醇反应的微观示意图(其中“○”代表氢原子,“
如图是工业上在一定条件下制取乙醇反应的微观示意图(其中“○”代表氢原子,“ ”代表碳原子,“
”代表碳原子,“ ”代表氧原子).下列叙述中,不正确的是( )
”代表氧原子).下列叙述中,不正确的是( )
 如图是工业上在一定条件下制取乙醇反应的微观示意图(其中“○”代表氢原子,“
如图是工业上在一定条件下制取乙醇反应的微观示意图(其中“○”代表氢原子,“ ”代表碳原子,“
”代表碳原子,“ ”代表氧原子).下列叙述中,不正确的是( )
”代表氧原子).下列叙述中,不正确的是( )| A. | 反应物A的化学符号为2CH2 | |
| B. | 反应前后三种物质的分子个数比为1:1:1 | |
| C. | 乙醇中碳、氢、氧三种元素的质量比为12:3:8 | |
| D. | 1个乙醇分子由1个氧原子、2个碳原子、6个氢原子构成 |
1.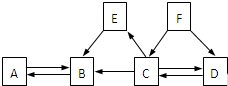 几种常见物质之间的相互转化关系如图所示,已知常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体,都由两种相同的元素组成,且分子中原子个数比依次为2:1和1:1;E为黑色固体,与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去).下列有关判断正确的是( )
几种常见物质之间的相互转化关系如图所示,已知常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体,都由两种相同的元素组成,且分子中原子个数比依次为2:1和1:1;E为黑色固体,与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去).下列有关判断正确的是( )
 几种常见物质之间的相互转化关系如图所示,已知常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体,都由两种相同的元素组成,且分子中原子个数比依次为2:1和1:1;E为黑色固体,与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去).下列有关判断正确的是( )
几种常见物质之间的相互转化关系如图所示,已知常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体,都由两种相同的元素组成,且分子中原子个数比依次为2:1和1:1;E为黑色固体,与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去).下列有关判断正确的是( )| A. | E转变为B一定是置换反应 | |
| B. | A不一定是H2CO3 | |
| C. | D、F中相同元素的化合价不一定相同 | |
| D. | 除去B中混有的少量C,可以将混合气体通过盛有NaOH溶液的洗气瓶 |