题目内容
12.用含有二氧化碳和水蒸气杂质的某种还原性气体测定一种铁的氧化物(FexOy)的组成,实验装置如图所示: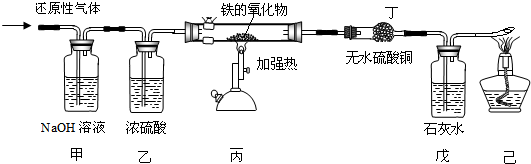
根据图回答:
(1)乙装置的作用是吸收水蒸气.
(2)实验过程中丁装置中没有明显的变化,而戊装置中出现了白色沉淀,则该还原性气体是一氧化碳.
(3)戊中发生反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O.
(4)上述实验中,如果没有甲装置,将使测定结果中铁元素与氧元素的质量比偏小(填“偏大”“偏小”或“无影响”)
(5)如果没有乙装置,可能产生的结果是不能排除还原性气体中含有氢气.
分析 氢氧化钠溶液能够吸收二氧化碳气体,浓硫酸能够吸收水蒸气;
水能和无水硫酸铜反应生成五水硫酸铜,二氧化碳能使澄清石灰水变浑浊;
高温条件下,铁的氧化物能和氢气反应生成铁和水;
如果操作不当,会影响实验结果,甚至会导致实验失败.
解答 解:(1)乙装置的作用是吸收水蒸气.
故填:吸收水蒸气.
(2)实验过程中丁装置中没有明显的变化,说明反应没有生成水,即还原性气体不是氢气,而戊装置中出现了白色沉淀,是因为反应生成了二氧化碳,因此该还原性气体是一氧化碳.
故填:一氧化碳.
(3)戊中二氧化碳和氢氧化钙发生反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:Ca(OH)2+CO2═CaCO3↓+H2O.
(4)上述实验中,如果没有甲装置,会导致产生的二氧化碳质量偏大,从而导致计算的铁的氧化物中氧元素质量偏大,进一步导致测定结果中铁元素与氧元素的质量比偏小.
故填:偏小.
(5)如果没有乙装置,从溶液中带出的水蒸气会进入丁中,导致白色无水硫酸铜变成蓝色固体,从而无法确定气体中是否含有氢气.
故填:不能排除还原性气体中含有氢气.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
2.烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g.某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量记录如下:
(1)该混合溶液中硫酸铜的质量为16g.
(2)参加反应的NaOH溶液的总质量是多少?
| 加入NaOH溶液的质量/g | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| 生成沉淀的质量/g | 0.0 | 2.5 | 8.6 | 9.8 | 9.8 |
(2)参加反应的NaOH溶液的总质量是多少?
17.第十一届全国运动会将于2009年10月在山东济南开幕.济南是以泉城而闻名.为了全运会的顺利召开,保护环境,人人有责.下列做法,与环境保护的倡导不相符的是( )
①污水排入大明湖;
②随意丢弃方便袋;
③植树种花搞绿化;
④禁用含磷洗衣粉;
⑤护城河旁烧垃圾.
①污水排入大明湖;
②随意丢弃方便袋;
③植树种花搞绿化;
④禁用含磷洗衣粉;
⑤护城河旁烧垃圾.
| A. | ①⑤ | B. | ①③ | C. | ①②⑤ | D. | ③④ |
1.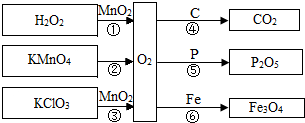 如图是氧气的制取和性质的相关知识网络(反应条件部分省略),下列有关说法不正确的是( )
如图是氧气的制取和性质的相关知识网络(反应条件部分省略),下列有关说法不正确的是( )
 如图是氧气的制取和性质的相关知识网络(反应条件部分省略),下列有关说法不正确的是( )
如图是氧气的制取和性质的相关知识网络(反应条件部分省略),下列有关说法不正确的是( )| A. | C、P、Fe均可在空气中燃烧 | B. | 反应①③中MnO2的作用均为催化作用 | ||
| C. | 反应①②③均属于分解反应 | D. | 反应④⑤⑥的生成物均为氧化物 |

 正确的实验操作对实验结果很重要.在实验课上,老师要求学生配制10%的氢氧化钠溶液50.0g.
正确的实验操作对实验结果很重要.在实验课上,老师要求学生配制10%的氢氧化钠溶液50.0g.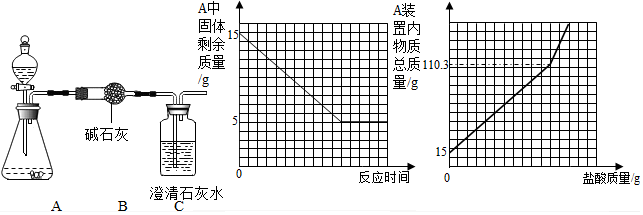

 某同学准备进行常见酸、碱、盐的性质实验时,发现实验台上有一瓶标签破损的溶液(如图),已知它是氯化钠溶液、氢氧化钠溶液、碳酸钠溶液三者中的一种,于是决定对这瓶溶液进行实验探究.
某同学准备进行常见酸、碱、盐的性质实验时,发现实验台上有一瓶标签破损的溶液(如图),已知它是氯化钠溶液、氢氧化钠溶液、碳酸钠溶液三者中的一种,于是决定对这瓶溶液进行实验探究.